 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知$(Zn2+,Zn)=-0.763V,$(Fe2+,Fe)=-0.440V。这两电极排成自发电池时,E$=()V,当有2mol电子的电量输出时,电池反应的K$=()。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“已知$(Zn2+,Zn)=-0.763V,$(Fe2+,Fe)=-0.440V。这两电极排成自发电池时,E$=()V,当有2mol电子的电量输出时,电池反应的K$=()。”相关的问题
更多“已知$(Zn2+,Zn)=-0.763V,$(Fe2+,Fe)=-0.440V。这两电极排成自发电池时,E$=()V,当有2mol电子的电量输出时,电池反应的K$=()。”相关的问题
第1题
经计算判断反应Zn2+(0.10mol·L-1)+Cu====Zn+Cu2+(2.0mol·L-1)的方向。已知

第2题
在0.50mol·L-1H2SO4溶液中电解1.00×10-3mol·L-1ZnSO4溶液,锌是否可在镀锌的铂电极上析出?如果介质c(H+)=1.00×10-5mol·L-1时,锌是否能析出?已知,在锌电极上η(H2)=-0.70V,
第3题
电解1.000×10-2mol·L-1硫酸锌溶液,当介质为0.50mol·L-1硫酸溶液时,锌是否能在铂电极上析出?如果介质[H<sup>+</sup>]=10-5mol·L-1时,锌是否能析出?(在锌电极上,ηH2=-0.70V;E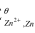 (zn2+/zn)=-0.763V)
(zn2+/zn)=-0.763V)
第4题
已知原电池(-)Zn|Zn2+(0.5mol·mol-1)||OH-(1.0mol·mol-1)|O2(200kPa)|Pt(),
第5题
A.正确
B.错误
第7题
在一块Ag板和一块Zn板中加入1.0mol·L-1K2CO3凝胶组成一个蓄电池。已知

第8题
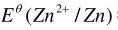 =0.76V,
=0.76V, =0.799V,该电池的标准电动势:()
=0.799V,该电池的标准电动势:()A.1.180V
B.0.076V
C.0.038V
D.1.559V
第9题
已知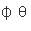 (Zn2+/Zn)=-0.762V,
(Zn2+/Zn)=-0.762V,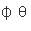 (Cu2+/Cu)=0.342V,[Zri(NH3)4]2+的Ks=2.9×109,[Cu(NH3)4]2+的Ks=2.1×1013。计算下列电池的电动势:
(Cu2+/Cu)=0.342V,[Zri(NH3)4]2+的Ks=2.9×109,[Cu(NH3)4]2+的Ks=2.1×1013。计算下列电池的电动势:
(-)Zn|[Zn(NH3)4]2+(0.100mol·L-1),NH3·H2O(1.00mol·L-1)‖NH3·H2O(1.00mol·L-1),[Cu(NH3)4]2+(0.100mol·L-1)|Cu()
第10题
已知原电池(-)Zn(s)|Zn2+(1mol·L-1)‖KCl(饱和)|Hg2Cl2(s),Hg(l)()。则该电池的正极反应是______;负极反应是______。
第11题
1mol·L-1的Na2CO3溶液中,逐滴加入Zn2+溶液,计算说明是先生成Zn(OH)2沉淀,还是先生成ZnCO3沉淀(忽略体积变化)。已知:


