 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于银锌电池:(-)Zn|Zn2+(1mol·L-1)||Ag+(1mol·L-1)|Ag(),已知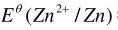 =0.76V,
=0.76V, =0.799V,该电池的标准电动势:()
=0.799V,该电池的标准电动势:()
A.1.180V
B.0.076V
C.0.038V
D.1.559V
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
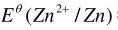 =0.76V,
=0.76V, =0.799V,该电池的标准电动势:()
=0.799V,该电池的标准电动势:()A.1.180V
B.0.076V
C.0.038V
D.1.559V
 答案
答案
 更多“对于银锌电池:(-)Zn|Zn2+(1mol·L-1)||Ag+(1mol·L-1)|Ag(+),已知=0.76V,=0.799V,该电池的标准”相关的问题
更多“对于银锌电池:(-)Zn|Zn2+(1mol·L-1)||Ag+(1mol·L-1)|Ag(+),已知=0.76V,=0.799V,该电池的标准”相关的问题
第1题
含银电极的AgNO3溶液通过盐桥与含有锌电极的Zn(NO3)2溶液相连,这一电池的符号是______。
第2题
第3题
A.正确
B.错误
第4题
已知原电池(-)Zn(s)|Zn2+(1mol·L-1)‖KCl(饱和)|Hg2Cl2(s),Hg(l)()。则该电池的正极反应是______;负极反应是______。
第5题
称取纯金属锌0.6539g,溶于HCl后,定量转移并稀释到500mL容量瓶中,定容,摇匀,计算溶液中Zn2+的摩尔浓度。已知M(Zn)=65.39g/mol。
第7题
A.电池反应:Zn+Cu2+↔Zn2++Cu
电极反应:正极:Zn-2e↔Zn2+
负极:Cu2++2e↔Cu
B.电池反应:Zn+Cu2+↔Zn2++ Cu
电极反应:正极:Cu2++2e↔Cu
负极:Zn-2e↔Zn2+
C.电池反应:Zn2++Cu↔Zn+Cu2+
电极反应:正极:Cu2++2e↔Cu
负极:Zn-2e↔Zn2+
D.电池反应:Zn2++Cu↔Zn+Cu2+
电极反应:正极:Zn-2e↔Zn2+
负极:Cu2++2e↔Cu
第8题
已知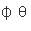 (Zn2+/Zn)=-0.762V,
(Zn2+/Zn)=-0.762V,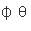 (Cu2+/Cu)=0.342V,[Zri(NH3)4]2+的Ks=2.9×109,[Cu(NH3)4]2+的Ks=2.1×1013。计算下列电池的电动势:
(Cu2+/Cu)=0.342V,[Zri(NH3)4]2+的Ks=2.9×109,[Cu(NH3)4]2+的Ks=2.1×1013。计算下列电池的电动势:
(-)Zn|[Zn(NH3)4]2+(0.100mol·L-1),NH3·H2O(1.00mol·L-1)‖NH3·H2O(1.00mol·L-1),[Cu(NH3)4]2+(0.100mol·L-1)|Cu()
第9题
在0.50mol·L-1H2SO4溶液中电解1.00×10-3mol·L-1ZnSO4溶液,锌是否可在镀锌的铂电极上析出?如果介质c(H+)=1.00×10-5mol·L-1时,锌是否能析出?已知,在锌电极上η(H2)=-0.70V,
第10题
湿法炼锌过程中,假设由于电解液含铁太多,锌极表面有1%被铁覆盖,当锌极维持在-0.8V(vs SHE)时,估算锌沉积过程的电流效率。氢离子放电和金属锌沉积的阴极极化曲线如图所示,
(1)Zn|H2,0.5mol·L-1H2S04,20℃;
(2)Zn|Zn2+,0.5mol·L-1H2S04,20℃;
(3)Fe|H2,0.5mol·L-1,H2S04,20℃。

习题8.2
第11题
电解1.000×10-2mol·L-1硫酸锌溶液,当介质为0.50mol·L-1硫酸溶液时,锌是否能在铂电极上析出?如果介质[H<sup>+</sup>]=10-5mol·L-1时,锌是否能析出?(在锌电极上,ηH2=-0.70V;E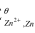 (zn2+/zn)=-0.763V)
(zn2+/zn)=-0.763V)