 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应Cu2+(aq)+Zn(s)=Cu(S)+Zn2+在标准状态下正向自发,原因为:
A.Zn的电离能较小;
B.Cu的电子亲合能较大;
C.Cu的电负性较大;
D.Zn抖/Zn的标准电极电势低于Cu抖/Cu的标准电极电势。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Zn的电离能较小;
B.Cu的电子亲合能较大;
C.Cu的电负性较大;
D.Zn抖/Zn的标准电极电势低于Cu抖/Cu的标准电极电势。
 答案
答案
 更多“反应Cu2+(aq)+Zn(s)=Cu(S)+Zn2+在标准状态下正向自发,原因为: A.Zn的电离能较小; B.Cu的电子亲合能较大;”相关的问题
更多“反应Cu2+(aq)+Zn(s)=Cu(S)+Zn2+在标准状态下正向自发,原因为: A.Zn的电离能较小; B.Cu的电子亲合能较大;”相关的问题
第1题
电池Zn|znSO4(aq)||CuSO4(aq)|Cu对外放电时,锌极进行_________反应,是________极(填正、负),电极反应是_______。
第2题
完成并配平下列用于定性分析的反应方程式: (a)As2O3(s)+Zn(s)+HCl(aq)→
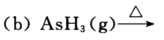 (c)AsH3(g)+AgNO3(aq)+H2O(1)→ (d)HgCl2(aq)+SnCl2(aq)→ (e)Hg2Cl2(s)+SnCl2(aq)→ (f)Bi(OH)3(s)+[Sn(OH)4]2-(aq)→
(c)AsH3(g)+AgNO3(aq)+H2O(1)→ (d)HgCl2(aq)+SnCl2(aq)→ (e)Hg2Cl2(s)+SnCl2(aq)→ (f)Bi(OH)3(s)+[Sn(OH)4]2-(aq)→
第3题
目前正在研究的锌氯电池是一种可能成为电动汽车发动机能源的新型电池。该电池的电池反应如下所示:Zn(s)+Cl2(g)→ZnCl2(aq)。试求该电池电动势。
第5题
用氧化值法配平下列反应方程式: (a)SiO2(s)+Al(s)→Si(s)+Al2O3(s) (b)I2(s)+H2S(aq)→I-(aq)+S(s)+H2O+(aq) (c)H2O2(aq)+I-(aq)+H3O+(aq)→I2(s)+H2O(l) (d)H2S(g)+O2(g)→O2(g)+H2O(g) (e)NH3(g)+O2(g)→NO2(g)+H2O(g) (f)SO2(g)+H2S(g)→S8(s)+H2O(g) (g)HNO3(aq)+Cu(s)→Cu(NO3)2(aq)+NO(g)+H2O(l) (h)Ca3(PO4)2(s)+C(s)+SiO2(s)→CaSiO3(l)+P4(g)+CO(g) (i)KClO3(s)→KClO4(s)+KCl(s)(提示:歧化反应可方便地从反方向进行配平)
第6题
第7题
14.Write the notation for a cell in which the electrode reactions are
2H+(aq)+2e→H2(g)
Zn(s)→Zn2+(aq)+2e
第8题
Write the notation for a cell in which the electrode reactions are
2H+(aq)+2e→H2(g)
Zn(s)→Zn2+(aq)+2e
第9题
请分析在电极中加入NH3,以下电极电势如何变化? (1)Zn(s)丨Zn2+(aq); (2)CrO42-(ap),Cr3+(aq); (3)Fe2+(aq),Fe3+(aq)。
第10题
反应Cu+2Fe3+→Cu2++2Fe2+正向进行,说明Fe3+的氧化性大于Cu2+,金属Cu的还原性大于Fe2+。( )
第11题
已知
A.呈平衡态 B.正向自发进行 C.逆向自发进行