 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
原电池(-)Zn|Zn2+(1 mol.L-1)‖Cu2+(1 mol.L-1)I Cu()中,单质Cu既是电子的导体,又作为原电池的电极和还原剂。 ()此题为判断题(对,错)。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“原电池(-)Zn|Zn2+(1 mol.L-1)‖Cu2+(1 mol.L-1)I Cu()中,单质Cu既是电子的导体,又作为原电池的电”相关的问题
更多“原电池(-)Zn|Zn2+(1 mol.L-1)‖Cu2+(1 mol.L-1)I Cu()中,单质Cu既是电子的导体,又作为原电池的电”相关的问题
第1题
请分析在电极中加入NH3,以下电极电势如何变化? (1)Zn(s)丨Zn2+(aq); (2)CrO42-(ap),Cr3+(aq); (3)Fe2+(aq),Fe3+(aq)。
第2题
在





第3题
湿法炼锌过程中,假设由于电解液含铁太多,锌极表面有1%被铁覆盖,当锌极维持在-0.8V(vs SHE)时,估算锌沉积过程的电流效率。氢离子放电和金属锌沉积的阴极极化曲线如图所示,
(1)Zn|H2,0.5mol·L-1H2S04,20℃;
(2)Zn|Zn2+,0.5mol·L-1H2S04,20℃;
(3)Fe|H2,0.5mol·L-1,H2S04,20℃。

习题8.2
第4题
14.Write the notation for a cell in which the electrode reactions are
2H+(aq)+2e→H2(g)
Zn(s)→Zn2+(aq)+2e
第5题
A.正确
B.错误
第7题
称取纯金属锌0.6539g,溶于HCl后,定量转移并稀释到500mL容量瓶中,定容,摇匀,计算溶液中Zn2+的摩尔浓度。已知M(Zn)=65.39g/mol。
第8题
A.负极是Cu,发生氧化反应;正极是Zn,发生还原反应
B.负极是Cu,发生还原反应;正极是Zn,发生氧化反应
C.负极是Zn,发生氧化反应;正极是Cu,发生还原反应
D.负极是Zn,发生还原反应;正极是Cu,发生氧化反应
第9题
将0.167 5 g铁配制成100.00mL FeS04溶液,用0.100 0 mol. L -1 Ce(S04)2标准溶液滴定。铂电极作指示电极,SCE电极作参比电极,当加入20.00 mL Ce(SO4):标准溶液时,电池的电动势是多少?化学计量点的电动势是多少?
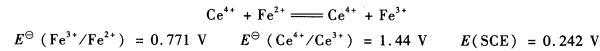
第10题
Evaporation rates of hydrocarbon liquid from horizontal surfaces are approximately given by
Where p is vapor pressure of the liquid and P is the atmospheric pressure. We have spilled a layer of lubricating oil on a metal drip pan in our garage. It forms a layer 1 mm thick. Its density is 1g/cm3and its molecular weight is 400 g/mol. Its vapor pressure is approximately 10-7torr at 20℃. Estimate how long it will take all of this motor oil to evaporate at 20℃.