 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于可逆反应C(s)+H2O(g)====CO(g)+H2(g),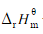 >0。下列说法正确的是:
>0。下列说法正确的是:
A.达到平衡时,p(H2O)=p(CO)=p(H2),即反应物与生成物压力相等;
B.达到平衡后,p(H2O)、p(CO)、p(H2)不再改变;
C.由于反应前后分子数目相等,所以增加压力对平衡没有影响;
D.升高温度,平衡逆向移动。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
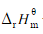 >0。下列说法正确的是:
>0。下列说法正确的是:A.达到平衡时,p(H2O)=p(CO)=p(H2),即反应物与生成物压力相等;
B.达到平衡后,p(H2O)、p(CO)、p(H2)不再改变;
C.由于反应前后分子数目相等,所以增加压力对平衡没有影响;
D.升高温度,平衡逆向移动。
 答案
答案
 更多“对于可逆反应C(s)+H2O(g)====CO(g)+H2(g),>0。下列说法正确的是: A.达到平衡时,p(H2O)=p(CO)=p(H2),即反应”相关的问题
更多“对于可逆反应C(s)+H2O(g)====CO(g)+H2(g),>0。下列说法正确的是: A.达到平衡时,p(H2O)=p(CO)=p(H2),即反应”相关的问题
第1题
 Co(g)+H2(g)的△H=-121.3kJ·mol-1,下列说法中正确的是( )。
Co(g)+H2(g)的△H=-121.3kJ·mol-1,下列说法中正确的是( )。A.达平衡时各反应物和生成物的浓度相等
B.加入催化剂可以加快反应达平衡的时间
C.增加压力对反应速率和平衡均无影响
D.升高温度,正反应速率增大,逆反应速率减小,结果平衡向右移动
第3题
 CO(g)+H2O(g)在673K和873K时的标准平衡常数分别为8.0>(10—2和0.4),由此可知正向反应是吸热反应。()此题为判断题(对,错)。
CO(g)+H2O(g)在673K和873K时的标准平衡常数分别为8.0>(10—2和0.4),由此可知正向反应是吸热反应。()此题为判断题(对,错)。第4题
下述两反应哪一个反应过程中放出的热量较大?为什么?
(a)A(g)+B(s)→C(l)+H2O(g)
(b)A(g)+B(s)→C(l)+H2O(l)
第5题
 计算的是( )。
计算的是( )。A.H2O(s,-11℃)→H2O(1,10℃)
B.H2O(1,100℃)→H2O(g,100℃)
C.H2O(1,90℃)→H2O(g,90℃)
D.H2O(s,0℃)→H2O(g,8℃)
第6题
下述两反应哪一个反应过程中放出的热量较大?为什么? (a)A(g)+B(s)→C(1)+H2O(g) (b)A(g)+B(s)→C(1)+H2O(1)
第7题
反应C(s)+H2O(g)=CO(g)+H2(g),为提高C(s)的转化率,可采取()措施。
A.增加C(s)的用量
B.增加H2O(g)的浓度
C.按1:1增加,C(s)和H2O(g)的用量
D.以上三种方法都可以
第8题
 H2(g)+FeO(s)====H2O(g)+Fe(g)
H2(g)+FeO(s)====H2O(g)+Fe(g) 则反应CO(g)+FeO(s)====Fe(g)+CO2(g)
则反应CO(g)+FeO(s)====Fe(g)+CO2(g) ( )。
( )。A.m+n
B.m-n
C.m×n
D.n/m
第9题
用氧化值法配平下列反应方程式: (a)SiO2(s)+Al(s)→Si(s)+Al2O3(s) (b)I2(s)+H2S(aq)→I-(aq)+S(s)+H2O+(aq) (c)H2O2(aq)+I-(aq)+H3O+(aq)→I2(s)+H2O(l) (d)H2S(g)+O2(g)→O2(g)+H2O(g) (e)NH3(g)+O2(g)→NO2(g)+H2O(g) (f)SO2(g)+H2S(g)→S8(s)+H2O(g) (g)HNO3(aq)+Cu(s)→Cu(NO3)2(aq)+NO(g)+H2O(l) (h)Ca3(PO4)2(s)+C(s)+SiO2(s)→CaSiO3(l)+P4(g)+CO(g) (i)KClO3(s)→KClO4(s)+KCl(s)(提示:歧化反应可方便地从反方向进行配平)
第10题
Calculate the values of
第11题
计算1000℃下水煤气合成反应的△H和△G。
C(s)+H2O(g)====CO(g)+H2(g)
组分 | a | b | c | Delta H_f^{ominus } | Delta G_f^{ominus } |
C(s) | 14.72 | 6.41 | 7.21 | ||
H2O(g) | 28.85 | 12.06 | 1.01 | -241.818 | -228.572 |
CO(g) | 28.07 | 4.63 | -0.26 | 110.525 | -137.169 |
H2(g) | 27.01 | 3.51 | 0.69 |
各物质的摩尔恒压热容计算式为的状态都是指的298K和101.325kPa,单位为J·mol-1。