 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知某Bi3+、Pb2+混合溶液中,cBi=cPb=0.02000mol•L-1,欲用同浓度的EDTA标准溶液连续滴定。a.连续滴定的可行性如何?b.控制溶液的pH=1.0,能否准确滴定Bi3+?c.滴定Pb2+的适宜酸度范围是多少?采用何种缓冲溶液?d.解释选用二甲酚橙作为Bi3+、Pb2+连续滴定的指示剂的原理。
 答案
答案


 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案


 更多“已知某Bi3+、Pb2+混合溶液中,cBi=cPb=0.02000mol•L-1,欲用同浓度的EDTA标准溶液连续滴定。a.连续滴定的可行性如何?b.控制溶液的pH=1.0,能否准确滴定Bi3+?c.…”相关的问题
更多“已知某Bi3+、Pb2+混合溶液中,cBi=cPb=0.02000mol•L-1,欲用同浓度的EDTA标准溶液连续滴定。a.连续滴定的可行性如何?b.控制溶液的pH=1.0,能否准确滴定Bi3+?c.…”相关的问题
第1题
已知lg



第2题
在相同浓度的Pb2+、Ba2+(均为0.1mol/L)的混合溶液中逐滴加入K2CrO4溶液(溶液体积变化忽略不计),先沉淀的物质是___。已知Kspθ(PbCrO4)=2.8×10-13,Kspθ(BaCrO4)=1.17×10-10。
A、PbCrO4
B、BaCrO4
C、不能确定
第3题
在298K时,将含有Sn(ClO4)2和Pb(ClO4)2的某溶液与过量的粉末状Sn-Pb合金一起振荡后,测得溶液中平衡浓度之比[Pb2+]/[Sn2+]为0.46。已知
 =-0.126V,计算
=-0.126V,计算
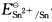 值。
值。
第5题
在含有 的混合溶液中,逐滴加入含Pb2+的溶液,当PbCrO4和PbSO4共同沉淀时,溶液中
的混合溶液中,逐滴加入含Pb2+的溶液,当PbCrO4和PbSO4共同沉淀时,溶液中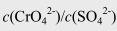 为( )
为( )

第6题
Ag+、Pb2+、Ba2+混合溶液中,各离子浓度均为0.010mol·L-1,向其中逐滴加入K2CrO4溶液,最先生成______沉淀,最后生成______沉淀。 (Ag2CrO4)=1.1×10-12,
(Ag2CrO4)=1.1×10-12, (BaCrO4)=1.2×10-10,
(BaCrO4)=1.2×10-10, (PbCrO4)=1.8×10-14
(PbCrO4)=1.8×10-14
第7题
用控制电位法分离Pb2+和Ni2+混合溶液中的Pb2+,试求: (1)若起始浓度[Pb2+]=[Ni2+]=0.100 0 mol?L-1,要使Pb2+沉积析出,阴极电位应控制在什么范围(vs.SHE)? (2)在(1)中所选定的电位上,计算残留在溶液中未被电解的Pb2+的分数为多少? (3)在(1)中所选定的电位上,要使30 mL混合试样中的Pb2+完全沉积析出,需要通入电量为多少库仑?
第10题
3.20×10-4mol·L-1Pb2+溶液的扩散电流为3.70μA,将此溶液与未知液等体积混合,测得扩散电流为10.2μA。计算未知液中Pb2+的浓度。
第11题
已知某溶液由两种物质组成,cA为物质A的质量浓度/g·L-1,cB为物质B的质量浓度/g·L-1,μ为物质的黏度/cP。设此溶液黏度的数学模型为
μ=a0+a1cA+a2cB
试根据下列实验数据,确定的a0、a1、a2值(1cP=1mPa·s)。
| cA/g·L-1 | cB/g·L-1 | μ/cP |
| 25.8 15.8 18.1 13.3 20.1 10.1 17.1 21.0 23.7 11.2 10.2 16.4 15.9 8.0 26.0 | 98 116 104 99 153 98 103 112 113 80 87 138 98 102 155 | 14.5 9.7 11.3 26.0 44.7 21.0 25.2 13.7 38.5 5.8 17.7 40.0 17.1 3.0 37.3 |