 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
碘化氢的分解反应为均相二级反应 2HI(g)=H2(g)+I2(g) 已知反应的活化能Ea为185kJ.
碘化氢的分解反应为均相二级反应 2HI(g)=H2(g)+I2(g) 已知反应的活化能Ea为185kJ.mol-1,分子的碰撞直径为3.50×10-10m。试确定反应速率常数kHI与温度的关系式并求556K时的反应速率常数。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
碘化氢的分解反应为均相二级反应 2HI(g)=H2(g)+I2(g) 已知反应的活化能Ea为185kJ.mol-1,分子的碰撞直径为3.50×10-10m。试确定反应速率常数kHI与温度的关系式并求556K时的反应速率常数。
 答案
答案
 更多“碘化氢的分解反应为均相二级反应 2HI(g)=H2(g)+I2(g) 已知反应的活化能Ea为185kJ.”相关的问题
更多“碘化氢的分解反应为均相二级反应 2HI(g)=H2(g)+I2(g) 已知反应的活化能Ea为185kJ.”相关的问题
第1题
碘化氢分解反应:2HI→H2+I2,已知临界能Ec=183.92kJ/mol,HI的分子直径d=3.5×10-10m,摩尔质量为127.9g/mol。试由碰撞理论计算在不同温度下HI分解的速率常数k并和下列实验数据相比较。

第2题
碘化氢分解反应:2HI→H2+I2,已知临界能Ec=183.92kJ/mol,HI的分子直径d=3.5×10-10m,摩尔质量为127.9g/mol。试由碰撞理论计算在不同温度下HI分解的速率常数k并和下列实验数据相比较。
| T(K) k[m3/(mol·s)] | 556 3.52×10-10 | 666 2.20×10-7 | 781 3.95×10-5 |
第3题
碘化氢的分解反应为
H2+I2-2HI=0,
实验测得该反应的平衡恒量K用下式表示
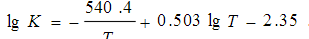 设在最初未发生分解时,除有N0mol的HI外,还同时有αN0mol的H2(这个问题称为有多余氢存在下HI的分解问题),又设I2不分解.试比较α=0与α=1两种情形在T=500K,1000K,1500K时的分解度
设在最初未发生分解时,除有N0mol的HI外,还同时有αN0mol的H2(这个问题称为有多余氢存在下HI的分解问题),又设I2不分解.试比较α=0与α=1两种情形在T=500K,1000K,1500K时的分解度

第4题
反应特性分析
实验表明氧化亚氨均相分解的反应为
速率表达式为
式中 k1=1019.39e-342251/(RT);
k2=108.69e-118826/(RT)。
问:(1)反应活化能为多少?
(2)分析反应特征。
第5题
宏观流体反应计算
试证明在一连续釜式反应器中进行的均相反应和宏观流体反应,当反应为一级不可逆时,其反应结果相同。
第6题
某化合物A的分解速率常数为0.29h-1,则此反应为______级反应,当c0=1.0mol·L-1时,此反应的半衰期为______,当c0=0.10mol·L-1时,此反应的半衰期为______。
第7题
SO3的分解反应为: 在200℃达到平衡时有48.5%分解了,在300℃达到平衡时有97%分解了,因此该反应的
在200℃达到平衡时有48.5%分解了,在300℃达到平衡时有97%分解了,因此该反应的
第9题
双乙酰气体受紫外线(λ=253.7nm)照射1.80×104S时,生成6.33×10-5mol.dm-3的CO,分解反应为
1.jpg) 被双乙酰吸收的紫外线强度为1.71×10-3J.dm-3.s-1。试求反应的量子效率。
被双乙酰吸收的紫外线强度为1.71×10-3J.dm-3.s-1。试求反应的量子效率。
第10题
下列反应中Kc=Kp的反应是()。
A.FeO(s)+CO(g)=Fe(s)+CO2(g)
B.H2(g)+I2(g)=2HI(g)
C.3NO2(g)+H2O(l)=2HNO3(l)+NO(g)
D.Cl2(g)+H2O(l)=2HClO(l)