 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03mol/L(除掉CN与Zn2+配合以外的总浓度)时,计算和
在![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
![在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03m](https://img2.soutiyun.com/latex/latex.action)
 答案
答案
 更多“在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03mol/L(除掉CN与Zn2+配合以外的总浓度)时,计算和”相关的问题
更多“在为1.0×10-2mol/L的溶液中,当[NH3]=0.17mol/L(pH=10)、=0.03mol/L(除掉CN与Zn2+配合以外的总浓度)时,计算和”相关的问题
第1题
下列所列滴定过程是用1.0×10-2mol/L的试剂滴定100mL 1.0×10-3mol/L的溶液。假定滴定过程的体积变化可以忽略,各种离子的摩尔电导和无限系数的摩尔电导无显著的差别,计算顺次加入0.0mL、4.0mL、10.0mL、16.0mL试剂之后溶液的电导率。
(1)用NaOH滴定HAc;(2)用氨滴定HAc;(3)用NaCl滴定AgNO3。
第2题
在NH3和
第3题
A、2.9³10-4mol/L
B、2.9³10-3mol/L
C、1.9³10-2mol/L
D、3.9³10mol/L
第4题
[H+]=10-5mol/L的溶液,pH=______,[OH-]=10-2mol/L的溶液,pH=______。
第5题
有一含NaClO3的未知溶液,取50.0ml以
第6题
测定在l×10-2mol·L-1CuS04+1mol·L-1H2S04溶液中的复数平面图,(1)极化前测得的;(2)ηK=14mV时测得的。问:(1)Cu2+还原为Cu的电极过程的控制步骤的特征;(2)解释两个复数平面图的图形。(可参考:《电镀与涂饰》,1986,(4),50)

习题9.7图
第7题
在0.10 mol?L-1HCIO4溶液中,以铂电极为阴极,电解1.000×10-2 mol?L-1 Cu2+和1.000×10-2mol?L-1Sn2+的混合溶液。试指出在阴极上离子的析出顺序。(已知
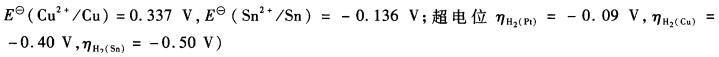
第8题
 =1.07×10-10。把BaSO4放入c(Na2SO4)=0.010mol·L-1Na2SO4溶液中,BaSO4的溶解度是( )。(不考虑副反应)
=1.07×10-10。把BaSO4放入c(Na2SO4)=0.010mol·L-1Na2SO4溶液中,BaSO4的溶解度是( )。(不考虑副反应)A.1.03×10-5mol·L-1
B.1.07×10-6mol·L-1
C.1.07×10-2mol·L-1
D.1.07×10-8mol·L-1
第9题
在间歇反应器中,于15℃等温条件下采用葡萄糖淀粉酶进行麦芽糖水解反应,Km=1.22×10-2mol/L,麦芽糖的初始浓度为2.58×10-3mol/L,反应10min测得麦芽糖转化率为30%,试计算麦芽糖转化率达90%时所需的反应时间。
第10题
某物质(x)的含量及其荧光相对强度(y)的关系如下:
| x含量/(μg/L) | 0.0 | 0.2 | 0.4 | 0.6 | 0.8 | 1.0 |
| 荧光相对强度y | 1.0 | 2.5 | 4.6 | 6.3 | 8.7 | 10.5 |
(1)请列出一元线性回归方程;(2)若含某物质x的未知溶液,测得其荧光相对强度y为1.5,求出未知液中x的含量。