 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一个电池反应确定的电池,E值的正或负可以用来说明()
A、电池是否可逆
B、电池反应是否已达平衡
C、电池反应自发进行的方向
D、电池反应的限度
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、电池是否可逆
B、电池反应是否已达平衡
C、电池反应自发进行的方向
D、电池反应的限度
 答案
答案
 更多“一个电池反应确定的电池,E值的正或负可以用来说明()”相关的问题
更多“一个电池反应确定的电池,E值的正或负可以用来说明()”相关的问题
第1题
电池Zn|znSO4(aq)||CuSO4(aq)|Cu对外放电时,锌极进行_________反应,是________极(填正、负),电极反应是_______。
第2题
在书写电池半反应时,可以有多种书写形式,如
①Ag2S+2e→2Ag+S2-
②1/2Ag2S+e→Ag+1/2S2-
③2Ag+S2-→Ag2S+2e
④Ag+1/2S2-→1/2Ag2S+e
无论采用何种形式,只要电极反应的条件相同,上述各电极反应的电势值均相同。
第3题
2.在书写电池半反应时,可以有多种书写形式,如
①Ag2S+2e→2Ag+S2-
②1/2Ag2S+e→Ag+1/2S2-
③2Ag+S2-→Ag2S+2e
④Ag+1/2S2-→1/2Ag2S+e
无论采用何种形式,只要电极反应的条件相同,上述各电极反应的电势值均相同。
第4题
 ,当离子的浓度均为0.5mol·L-1时,该电池的电动势为E,则下述关系存在的是( )。
,当离子的浓度均为0.5mol·L-1时,该电池的电动势为E,则下述关系存在的是( )。A.


第7题
现有电池Zn(s)|ZnCl2(m)|AgCl(s)|Ag(s),在下面的空格内选择阴、阳,正、负填入。作为原电池时,Zn电极是______极、______极;作为电解池时,Zn电极是______极、______极。
第8题
任何氧化还原电对的标准还原电位都是由半电池反应确定的。NAD+/NADH和丙酮酸/乳酸的标准还原电位分别为-0.32V和-0.19V。
第10题
在溶液中,反应Cd(CH3NH2)42++2NH2CH2CH2NH2====Cd(NH2CH2CH2NH2)22++4CH3NH2的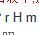 约为______kJ·mol-1,且此反应是熵______(增或减)反应,所以此反应的△rGm是______值(正或负),在______(高,低或任何)温度下,都是______(正向自发或正向不自发)。
约为______kJ·mol-1,且此反应是熵______(增或减)反应,所以此反应的△rGm是______值(正或负),在______(高,低或任何)温度下,都是______(正向自发或正向不自发)。