 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
现有电池Zn(s)|ZnCl2(m)|AgCl(s)|Ag(s),在下面的空格内选择阴、阳,正、负填入。作为原电池时,Zn电极是______极
现有电池Zn(s)|ZnCl2(m)|AgCl(s)|Ag(s),在下面的空格内选择阴、阳,正、负填入。作为原电池时,Zn电极是______极、______极;作为电解池时,Zn电极是______极、______极。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
现有电池Zn(s)|ZnCl2(m)|AgCl(s)|Ag(s),在下面的空格内选择阴、阳,正、负填入。作为原电池时,Zn电极是______极、______极;作为电解池时,Zn电极是______极、______极。
 答案
答案
 更多“现有电池Zn(s)|ZnCl2(m)|AgCl(s)|Ag(s),在下面的空格内选择阴、阳,正、负填入。作为原电池时,Zn电极是______极”相关的问题
更多“现有电池Zn(s)|ZnCl2(m)|AgCl(s)|Ag(s),在下面的空格内选择阴、阳,正、负填入。作为原电池时,Zn电极是______极”相关的问题
第1题
已知电池反应(-)zn|ZnCl2(aq)||PbCl2(s)|Pb()的标准电动势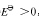 则反应
则反应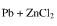
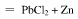 的标准平衡常数
的标准平衡常数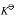 为
为
(A) 大于1 (B) 小于1 (C) 等于1 (D) 等于零
第3题
目前正在研究的锌氯电池是一种可能成为电动汽车发动机能源的新型电池。该电池的电池反应如下所示:Zn(s)+Cl2(g)→ZnCl2(aq)。试求该电池电动势。
第4题
已知Zn|ZnCl2(aq)|AgCl(s)|Ag的EΘ>0,则反应2Ag+ZnCl2=2AgCl+Zn的KΘ________I。(填>,=或<)
第5题
已知原电池(-)Zn(s)|Zn2+(1mol·L-1)‖KCl(饱和)|Hg2Cl2(s),Hg(l)()。则该电池的正极反应是______;负极反应是______。
第6题
298K时,某电池的E和EΘ分别为1.00V和1.10V,对应的电池反应为Zn(s)+Cu2+==Zn2++Cu(s)。下面哪种说法能正确解释E和EΘ的差别()
A.锌电极的电解质溶液为Zn(NO)3,铜电极的电解质溶液为CuSO4
B.Zn2+浓度大于Cu2+浓度
C.两半电池具有不同的体积
D.盐桥中的电解质为KCl
第7题
原子吸收光度法中,用标准加入法测定试液中Zn2+的含量。Zn2+标准贮备液由0.1043g ZnCl2溶于水,定量稀释至500mL配成。测定前将标准贮备液稀释10倍后使用,得以下数据。求:
| 序号 | 样品体积/mL | 加入标准溶液体积/mL | 稀释体积/mL | 吸光度 |
| 1 | 5.0 | 0.0 | 100 | 0.075 |
| 2 | 5.0 | 1.0 | 100 | 0.120 |
| 3 | 5.0 | 2.0 | 100 | 0.170 |
| 4 | 5.0 | 3.0 | 100 | 0.220 |
已知:Mr(ZnCl2)=136.3;Ar(Zn)=65.39。
第8题
Cu(s)|CuSO4(m')‖CuSO4(m")|Cu(s)浓差电池,m较小的一端为正极。
第9题
某电池反应为H2(100kPa)+Hg2Cl2(s)→2Hg(l)+2HCl(aq),298K时,当m(HCl)=10.0mol/kg时,E1=0.0322V,此时HCl的平衡分压为488Pa;当m(HCl)=1.1009mol/kg时,E2=0.399V,求此时HCl的平衡分压。
第10题
某电池反应为H2(100kPa)+Hg2Cl2(s)→Hg(1)+2HCl(aq),298K时,当m(HCl)=10.0mol/kg时,E1=0.0322V,此时HCl的平衡分压为488Pa;当m(HCl)=1.1009mol/kg时,E2=0.399V,求此时HCl的平衡分压。