 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在酸性介质中,已知,能发生歧化反应方程式为______,计算该反应的=______,298K时该反应的平衡常数为______。
在酸性介质中,已知,能发生歧化反应方程式为______,计算该反应的
=______,298K时该反应的平衡常数为______。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在酸性介质中,已知,能发生歧化反应方程式为______,计算该反应的
=______,298K时该反应的平衡常数为______。
 答案
答案
 更多“在酸性介质中,已知,能发生歧化反应方程式为______,计算该反应的=______,298K时该反应的平衡常数为______。”相关的问题
更多“在酸性介质中,已知,能发生歧化反应方程式为______,计算该反应的=______,298K时该反应的平衡常数为______。”相关的问题
第1题
已知
(A)
(B) 在标准状态时,反应 是自发进行的
是自发进行的
(C) 在酸性溶液中能发生歧化反应
(D) Fe与稀酸反应生成Fe2+和H2
第3题
MnO4¯0.564MnO42-2.26MnO20.95Mn2O3¯1.51Mn2+-1.18Mn
① 写出可能发生歧化反应的方程式,并配平。
② 写出MnO4¯ 作为氧化剂与Na2SO4在不同PH值下的反应。
第4题
第5题
根据下列事实,写出反应方程式:
(1)金属铜在空气中表面生成“铜绿”
(2)氯水中加入氢氧化钠,氯气味道消失
(3)高锰酸钾滴入酸性双氧水中,紫红色消失
(4)铜能溶解于稀硝酸中
(5)石灰岩溶洞及钟乳石的形成
(6)大苏打在纺织工业中常用作除氯剂
(7)变色硅胶常用作实验室的干燥剂
(8)泡沫灭火剂可高效灭火
第6题
下列物质的酸性水溶液(浓度均为1.0mol·dm-3),分别通入100kPa的氧气,能发生反应的是
已知: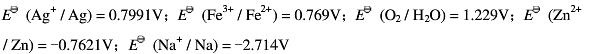 。
。
(A) AgNO3(B) ZnCl2(C) FeSO4(D) NaNO3
第7题
砷酸盐在酸性溶液中与I-作用,写出反应方程式;在该反应溶液中加入碱,反应进行的方向如何?
第10题
研究下列化学振荡:H2O2与KIO3在稀H2SO4溶液中的催化反应,在一定条件下,释放出O2的速率以及12的浓度会随时间呈周期性的变化。其主要反应(离子方程式)为(1)

当系统中有过量的H2O2参与并含有淀粉指示剂时,这种振荡能显示出蓝色和无色的周期性变化。请配平酸性溶液中进行的化学振荡(离子)反应(1)和(2),并说明其中H2O2所起的作用。
第11题
A. 在稀溶液中能全部电离出 H+ 的盐酸、硫酸和硝酸
B. 在稀溶液中能全部电离出弱酸,如氢硫酸和腐植酸
C.强碱弱酸生成的盐类,如 Na3CO 3、NaPO 4、醋酸钠。