 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
取10.0mL未知Zn2+试液于电解池中(其中含底液),在极谱仪上于1.25V的电压下进行电解,测得其波高为29.8mm。然后
取10.0mL未知Zn2+试液于电解池中(其中含底液),在极谱仪上于1.25V的电压下进行电解,测得其波高为29.8mm。然后加入1.00mL0.0200mol·L-1Zn2+标准溶液继续电解,测得其波高为57.8mm。由此可计算试液Zn2+的浓度c(Zn2+)=______。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
取10.0mL未知Zn2+试液于电解池中(其中含底液),在极谱仪上于1.25V的电压下进行电解,测得其波高为29.8mm。然后加入1.00mL0.0200mol·L-1Zn2+标准溶液继续电解,测得其波高为57.8mm。由此可计算试液Zn2+的浓度c(Zn2+)=______。
 答案
答案
 更多“取10.0mL未知Zn2+试液于电解池中(其中含底液),在极谱仪上于1.25V的电压下进行电解,测得其波高为29.8mm。然后”相关的问题
更多“取10.0mL未知Zn2+试液于电解池中(其中含底液),在极谱仪上于1.25V的电压下进行电解,测得其波高为29.8mm。然后”相关的问题
第1题
取30.0mL未知锌试液于电解池中,在极谱仪上于-1.25V的电压下进行电解,测得峰电流为30mA。在此溶液中加入1.00mL浓度为0.5000μg·mL-1的锌标准溶液,测得峰电流为50mA。计算样液中锌的浓度。
第2题
有一含NaClO3的未知溶液,取50.0ml以
第3题
某未知Ni2+试液,直流极谱法测得其波高为4.80mm(剩余电流已扣除)。加入0.50mL 1.00×10-3mol·L-1Ni2+标准溶液于25.00mL未知Ni2+试液中,测得其波高为7.20mm。计算该未知液中Ni2+的浓度。
第4题
用阳极溶出伏安法测定水样中的Pb2+、Cd2+、Cu2+含量。取水样4.00ml,加入到盛有46.0ml支持电解质溶液的电解池中,通2minN2,静置30s后将工作电极的电位向正方向扫描,测得Pb2+、Cd2+、Cu2+的溶出峰高分别为12mm、26mm、18mm。在上述溶液中加入0.10mlPh2+(10.00mg/L)、Cd2+(2.00mg/L)、Cu2+(5.00mg/L)的标准溶液,同样进行富集和溶出,测得溶出峰的峰高分别为20mm、45mm、32mm,试计算水样中Pb2+、Cd2+、Cu2+的含量。
第5题
A . 1.34×10-4
B . 2×10-4
C . 3.67×10-4
D . 4×10-4
第6题
原子吸收光度法中,用标准加入法测定试液中Zn2+的含量。Zn2+标准贮备液由0.1043g ZnCl2溶于水,定量稀释至500mL配成。测定前将标准贮备液稀释10倍后使用,得以下数据。求:
| 序号 | 样品体积/mL | 加入标准溶液体积/mL | 稀释体积/mL | 吸光度 |
| 1 | 5.0 | 0.0 | 100 | 0.075 |
| 2 | 5.0 | 1.0 | 100 | 0.120 |
| 3 | 5.0 | 2.0 | 100 | 0.170 |
| 4 | 5.0 | 3.0 | 100 | 0.220 |
已知:Mr(ZnCl2)=136.3;Ar(Zn)=65.39。
第8题
准确量取人体液试样10.0mL。为测定其中的钙含量,先把钙转化为CaC2O4沉淀。过滤、洗涤CaC2O4沉淀,然后用稀H2SO4溶解此沉淀,得到含H2C2O4溶液。再用浓度
第11题
电解1.000×10-2mol·L-1硫酸锌溶液,当介质为0.50mol·L-1硫酸溶液时,锌是否能在铂电极上析出?如果介质[H<sup>+</sup>]=10-5mol·L-1时,锌是否能析出?(在锌电极上,ηH2=-0.70V;E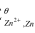 (zn2+/zn)=-0.763V)
(zn2+/zn)=-0.763V)