 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
确定由CO,CO2,H2,H2O,CH4组成混合物系统的独立反应数目,并写出反应式。
确定由CO,CO2,H2,H2O,CH4组成混合物系统的独立反应数目,并写出反应式。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
确定由CO,CO2,H2,H2O,CH4组成混合物系统的独立反应数目,并写出反应式。
 答案
答案
 更多“确定由CO,CO2,H2,H2O,CH4组成混合物系统的独立反应数目,并写出反应式。”相关的问题
更多“确定由CO,CO2,H2,H2O,CH4组成混合物系统的独立反应数目,并写出反应式。”相关的问题
第2题
甲烷水蒸气变换反应是生产合成气(主要是CO与H2)的一种途径,反应式如下:
CH4(g)+H2O(g)→CO(g)+3H2(g)CH4(g) + 2H2O(g) CO2(g) +4H2(g)
CO2(g) +4H2(g)
反应物预先加热至600K,最终产品的温度为1300K。如果反应进行完全,计算所需要的热量。
a | b | c | d | |
CH4 | 4.75 | 0.200×10-2 | 0.30×10-5 | 2.63×10-9 |
H2O | 7.70 | 0.046×10-2 | 0.25×10-5 | -0.86×10-9 |
CO | 6.73 | 0.400×10-2 | 0.13×10-5 | 0.53×10-9 |
H2 | 6.95 | -0.046×10-2 | 0.095×10-5 | -0.21×10-9 |
第3题
在900K,0.1013MPa下,用甲烷和水蒸气合成CO和H2时,常有副产物CO2存在。系统的反应式为:
 K1=2.053 (1)
K1=2.053 (1)
 K2=3.000 (2)
K2=3.000 (2)
若原料中CH4:H2O=1:1(mol),计算该反应的平衡组成。
第4题
写出由元素化合生成1molCH4(g)的化学方程式,由下列方程式和298.15K时的
(1)H2(g)+1/2O2(g)====H2O(l)
(2)C(s)+O2(g)====CO2(g)
(3)CH4(g)+2O2(g)====CO2(g)+2H2O(l)

第5题
写出由元素化合生成1 mol CH4(g)的化学方程式,由下列方程和293 K 时的△rHmθ值计算CH4的生成热。 H2(g)+
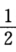 O2(g)→H2O(1) △rHmθ=一286.1 kJ.mol-1 C(s)+O2(g)→CO2(g) △rHmθ=一394.9 kJ.mol-1 CH4(g)+2O2(g)→CO2(g)+2H2O(1) △rHmθ=一882.0 kJ.mol-1
O2(g)→H2O(1) △rHmθ=一286.1 kJ.mol-1 C(s)+O2(g)→CO2(g) △rHmθ=一394.9 kJ.mol-1 CH4(g)+2O2(g)→CO2(g)+2H2O(1) △rHmθ=一882.0 kJ.mol-1
第6题
反应CO(g)+H2O(g)====CO2(g)+H2(g),当体系的压力增加一倍,平衡______移动。
第7题
 H2(g)+FeO(s)====H2O(g)+Fe(g)
H2(g)+FeO(s)====H2O(g)+Fe(g) 则反应CO(g)+FeO(s)====Fe(g)+CO2(g)
则反应CO(g)+FeO(s)====Fe(g)+CO2(g) ( )。
( )。A.m+n
B.m-n
C.m×n
D.n/m
第8题
反应CO(g)+H2O(g) CO2(g)+H2(g),在某温度时,
CO2(g)+H2(g),在某温度时,
第9题
已知下列反应在750℃时的
反应(1)
反应(2)H2(g)+CO2(g)====CO(g)+H2O(g)
求反应(3)

第10题
已知在25℃时: CO(g) CO2(g) H2O(g) △fCmθ/(kJ.mol-1) 一137.2 —394.4 —228.6 则反应CO(g)+H2O(g)===CO2(g)+H2(g) 在25℃和100 kPa下的△rGmθ=______________。
第11题
把密闭容器中的CO(g)和H2O(g)的混合物加热至476℃并达到如下平衡:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
已知该温度下反应的