 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知[Cu(OH)2]=2.0×10-20,(NH3·H2O)=1.8×10,{[Cu(
某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知![某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知[](https://img2.soutiyun.com/latex/latex.action)
![某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知[](https://img2.soutiyun.com/latex/latex.action)
![某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知[](https://img2.soutiyun.com/latex/latex.action)
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知![某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知[](https://img2.soutiyun.com/latex/latex.action)
![某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知[](https://img2.soutiyun.com/latex/latex.action)
![某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知[](https://img2.soutiyun.com/latex/latex.action)
 答案
答案
 更多“某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知[Cu(OH)2]=2.0×10-20,(NH3·H2O)=1.8×10,{[Cu(”相关的问题
更多“某溶液中含0.5mol·L-1NH3·H2O与0.1mol·L-1的[Cu(NH3)4]2+,已知[Cu(OH)2]=2.0×10-20,(NH3·H2O)=1.8×10,{[Cu(”相关的问题
第1题
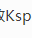 =1.8×10-5)溶液中加入NH4Cl固体,使c(NH4Cl)=0.2mol·L-1(忽略体积变化),此溶液的pH约为( )。
=1.8×10-5)溶液中加入NH4Cl固体,使c(NH4Cl)=0.2mol·L-1(忽略体积变化),此溶液的pH约为( )。A.4.35
B.9.65
C.5.15
D.8.35
第2题
用极谱法分析测定某0.200 g试样中Zn2+的质量分数。在0.1mol?L-1NH3一NH4Cl溶液中加入0.05%的动物胶及0.5%Na2SO3除氧,测得试样的极限扩散电流为41.7uA。与试样作同样处理的标准zn2+的质量及波高如下。计算试样中zn2+的质量分数。

第3题
微量稀土离子对铝合金的孔蚀有缓蚀作用,下表列出有SmCl3和无SmCl3时LYl2CZ铝合金在NaCl溶液中的腐蚀深度数据,试计算不同浸入时间的缓蚀效率。
0.5mol·L-1NaCl | 0.5mol·-1NaCl+1000ppmSmCl3 | |||||||
濅入时间/h | 120 | 240 | 480 | 720 | 120 | 240 | 480 | 720 |
腐蚀深度/h | 0.018 | 0.045 | 0.075 | 0.107 | 0.017 | 0.011 | 0.015 | 0.017 |
第4题
某H2O2溶液20.00mL酸化后与足量0.5mol·L-1KI溶液反应,用0.5000mol·L-1的Na2S2O3溶液滴定生成的I2,用去Na2S2O3溶液40.00mL。求H2O2溶液的浓度。
第5题
湿法炼锌过程中,假设由于电解液含铁太多,锌极表面有1%被铁覆盖,当锌极维持在-0.8V(vs SHE)时,估算锌沉积过程的电流效率。氢离子放电和金属锌沉积的阴极极化曲线如图所示,
(1)Zn|H2,0.5mol·L-1H2S04,20℃;
(2)Zn|Zn2+,0.5mol·L-1H2S04,20℃;
(3)Fe|H2,0.5mol·L-1,H2S04,20℃。

习题8.2
第6题
浓差电池的两个电极由金属X所组成,一个电极浸入浓度为0.5mol·dm-3相应的盐溶液中,另一个浸入浓度为0.05mol·dm-3相同盐的溶液中,298K时该电池的电动势为0.028v,请计算X的价数。
第7题
A、0.1mol/L的NaCl溶液
B、0.1mol/L的MgCl2溶液
C、0.1mol/L的AgNO3溶液
D、0.5mol/L的Na2SO4溶液
第8题
在0.5mol·L-1H2SO4介质中,测定混合离子溶液中各自的浓度。测定
的工作波长为440nm,测定
的工作波长为550nm,当比色皿厚度b=1.0cm时,对下述三种溶液测得的吸光度数值如下:
试样 | 浓度 C/mol·L-1 | 吸光度A (λ=440nm) | 吸光度A (λ=550nm) |
纯Cr_2O_7^{2-} | 8.73×10-4 | 0.308 | 0.009 |
纯MnO_4^- | 3.73×10-4 | 0.035 | 0.886 |
Cr_2O_7^{2-}+MnO_4^- | 未知 | 0.385 | 0.653 |
试计算未知液中各自的浓度。
第9题
已知: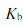 (NH3·H2O)=1.8×10-5,
(NH3·H2O)=1.8×10-5, (HAc)=1.8×10-5,按pH由大至小排列以下溶液(用序号排列)______。
(HAc)=1.8×10-5,按pH由大至小排列以下溶液(用序号排列)______。
①0.05mol·dm-3NH4Cl和0.05mol·L-1NH3·H2O混合液
②0.05mol·dm-3NaAc和0.05mol·L-1HAc混合液
③0.05mol·dm-3HAc
④0.05mol·dm-3NH3·H2O
⑤0.05mol·dm-3HCl溶液
⑥0.05mol·dm-3NaOH溶液
第10题
在某食品的消化液中加入1-2滴0.5mol/L的SnCl2,生成沉淀由白逐渐转灰或黑色,示有()。
A.Pb++
B.Hg++
C.Cu++
D.Mn++