 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知合成氨反应在25°C时的Kθp1为6.75×105,并知反应中各物质的标准熵值: N2(g)+3H2(g)= 2NH3 (g) S298θ(J.mol-1.K-1) 191.5 130.6 192.5 试计算(1)△rHmθ298; (2)500℃时的标准平衡常数Kθp2
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“已知合成氨反应在25°C时的Kθp1为6.75×105,并知反应中各物质的标准熵值: N2(g)+3H2(g)= 2NH3 (g) S298θ(J.mol-1.K-1) 191.5 130.6 192…”相关的问题
更多“已知合成氨反应在25°C时的Kθp1为6.75×105,并知反应中各物质的标准熵值: N2(g)+3H2(g)= 2NH3 (g) S298θ(J.mol-1.K-1) 191.5 130.6 192…”相关的问题
第1题
γ-羧基丁酸转化为γγ丁内酯的反应如下:
HOCHCHCHCOOH 该反应在25℃于0.2mol/L的盐酸中进行。已知羟基丁酸的初始浓度为18.23mol/dm,在不同时刻测得丁内酯的浓度如下:
t(min) | 0 | 21 | 36 | 50 | 65 | 80 | 100 | ∞ |
丁内酯浓度(mol/dm3) | 0 | 2.41 | 3.76 | 4.96 | 6.10 | 7.08 | 8.11 | 13.28 |
若正逆反应均为一级,试计算反应速度常数k1和k-1以及平衡常数K。
第2题
高温时,碘分子可解离为碘原子:I2(g)→2I(g)。已知该反应在1 473 K、1 173 K时的平衡常数之比为K1473/K1173=24.3,试计算I—I的键能。
第3题
合成氨的反应为:
热焓ΔH与温度T的关系如下:
| T/K | 623.0 | 648.0 | 637.0 | 698.0 | 723.0 | 748.0 | 773.0 |
| △H/kJ·mol-1 | -50.7879 | -51.13 90 | -51.4738 | -51.7943 | -52.1006 | -52.3929 | -52.6715 |
已知623K下的平衡常数Kp=2644Pa,求和773K下的平衡常数Kp。
第4题
已知反应 在25℃时,
在25℃时,


第5题
求证,反应速率常数为k的一级反应在两釜串联的反应器中的平均转化率为:
已知:两釜串联反应器的平均停留时间分布密度函数为:
其中,t为物料在每一釜中的平均停留时间。
第6题
合成氨反应 在450℃时平衡常数为0.073MPa-1。反应物料进料是物质的量配比为0.75H7:0.25N2的混合物,反应在450℃和40MPa下进行,近似假设各组分的逸度系数分别是
在450℃时平衡常数为0.073MPa-1。反应物料进料是物质的量配比为0.75H7:0.25N2的混合物,反应在450℃和40MPa下进行,近似假设各组分的逸度系数分别是

第7题
试求下列反应在1.013×105Pa及600K下的热效应
C3H8(g)+5O2→3CO2+4H4O(g)
已知有关参数及各气体的摩尔热容为






第8题
已知下列反应在750℃时的KΘ:
(1)(1/2)snO2(s)+H2(g)===(1/2)Sn(s)+H2O(g),
(2)H2(g)+CO2(g)===CO(g)+H2O(g),
求反应(3)(1/2)SnO2(s)+CO(g)===Sn(s)+CO2(g)在750℃的
第9题
已知N2+3H2=2NH3 Kp(673 K)=6.1×10-4。问此K户与下述3个K的意义是否相同?在进行合成氨反应的平衡计算时,是否可用任意一种Kp?
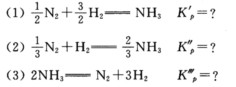
第10题
计算隔膜法氯碱电解槽的工作电压。已知:
(1) 电化学反应器中的反应如下。
阳极反应:2Cl-→Cl2+2e
阴极反应:2H2O+2e→2OH-+H2φ0=-0.828V
总反应:2H2O+2NaCl→2NaOH+Cl2+H2
(2) 反应在1500 A/m2和90℃条件下进行;
(3) 电极反应的过电位可用Tafel公式计算,即
阳极过电位:△φA=0.025+0.027lgi (i的单位为A/m2)
阴极过电位:△φK=0.113+0.056lgi
(4) 隔膜厚度为8mm,电阻率为0.035m·Ω;
(5) 电极间距离为9mm,电解液电导率为61.03m-1·Ω-1,充气率为0.2;
(6) 阳极液组成为320g/ NaCl(5.47mol/L),阴极液组成为100g/LNaOH(2.5mol/L);
(7) 第一类导体压降可忽略。
第11题
二级可逆反应动力学
在催化剂(HCl)的作用下,乙酸甲酯于25℃发生如下水解反应:
CH3COOCH3+H2O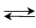 CH3COOH+CH3O 反应在25℃的平衡常数为0.22,乙酸甲酯和水的初始浓度分别为1.15mol/L和48.76mol/L。实验测得当反应进行到1h的时候,有34.92%的乙酸甲酯发生了水解。若正逆反应均为二级,试求反应速度常数k和k'。
CH3COOH+CH3O 反应在25℃的平衡常数为0.22,乙酸甲酯和水的初始浓度分别为1.15mol/L和48.76mol/L。实验测得当反应进行到1h的时候,有34.92%的乙酸甲酯发生了水解。若正逆反应均为二级,试求反应速度常数k和k'。