 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在酸性溶液中,与Mn2+反应生成MnO2沉淀,在分析Fe2+含量时却可由与Fe2+在酸性条件下定量反应。二者是否矛盾?
在酸性溶液中,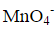 与Mn2+反应生成MnO2沉淀,在分析Fe2+含量时却可由
与Mn2+反应生成MnO2沉淀,在分析Fe2+含量时却可由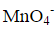 与Fe2+在酸性条件下定量反应。二者是否矛盾?
与Fe2+在酸性条件下定量反应。二者是否矛盾?
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在酸性溶液中,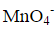 与Mn2+反应生成MnO2沉淀,在分析Fe2+含量时却可由
与Mn2+反应生成MnO2沉淀,在分析Fe2+含量时却可由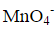 与Fe2+在酸性条件下定量反应。二者是否矛盾?
与Fe2+在酸性条件下定量反应。二者是否矛盾?
 答案
答案
 更多“在酸性溶液中,与Mn2+反应生成MnO2沉淀,在分析Fe2+含量时却可由与Fe2+在酸性条件下定量反应。二者是否矛盾?”相关的问题
更多“在酸性溶液中,与Mn2+反应生成MnO2沉淀,在分析Fe2+含量时却可由与Fe2+在酸性条件下定量反应。二者是否矛盾?”相关的问题
第1题
根据



(1)将适量高锰酸钾溶液滴加入强酸性的草酸钠溶液;
(2)将适量草酸钠溶液滴加入强酸性的高锰酸钾溶液。
第2题
<wt>“负,负”反应,在______温下正向自发,在______温下逆向自发。<w> <w>
<wt>M3+的3d轨道上有3个电子,表示这三个电子可能运动状态的4个量子数分别为______、______、______、______。<w> <w> <w> <w>
<wt>在电化学腐蚀中,被腐蚀的金属总是做______极,由于极化作用使被腐蚀的金属的φ值______,腐蚀速率减小。<w> <w>
<wt>将0.010dm3、1.0mol·dm-3的氨水和0.010dm3、0.333mol·dm-3的HCl溶液混合,混合液的pH值应为______。[已知
<wt>KMnO4的还原产物,在强酸性溶液中一般是______,在中性溶液中一般是______,在碱性溶液中一般是______。<w> <w> <w>
<wt>NCl3分子中,N原子采用______杂化,分子空间构型为______,分子间力为______。<w> <w> <w>
<wt>25℃时,若将0.010dm3、1.0mol·dm-3的CaCl2溶液和0.010dm3、0.20mol·dm-3的氨水混合后,溶液中c(OH-)=______mol·dm-3,反应商Q=[c(Ca2+)/c]·[c(OH-)/


<wt>若配合物[Pt(NH3)2Cl2]存在顺反异构体,则该配合物的空问构型为______,其中心离子的杂化轨道为______。<w> <w>
<wt>设元素A的原子序数为15,则其核外电子排布式为______,又设元素B原子序数为35,则作用于B原子最外层某一个电子上的有效核电荷数是______;AB3分子的空间构型为______。根据杂化轨道理论,A原子将采______杂化轨道与B原子成键。<w> <w> <w> <w>
<-->
<da>△rHm<0 <da><a>增大 <a>增大 <da>(3)<(1)<(5)<(6)<(2)<(4)
<da><a>浓差 <a>0 <a>0.03V <da>0.52 <da>-0.257V <da><a>5 <a>3
<da><a>1s22s22p63s23p63d54s2<a>d <a>4 <a>ⅦB <a>+7 <a>3s23p63d5
<da><a>sp3<a>sp <a>不等性sp3(或sp3) <a>不等性sp3<da><a>微生物 <a>隔绝氧气
<da><a>低 <a>高
<da><a>3 <a>2 <a>0 <a>1/2
<da><a>阳 <a>升高
<da>9.55
<da><a>Mn2+<a>MnO2<a>
<da><a>不等性sp3杂化 <a>三角锥型 <a>取向力、诱导力、色散力
<da><a>1.33×10-3<a>8.85×10-7<a>无
<da><a>平面正方型 <a>dsp2
<da><a>1s22s22p63s23p3<a>7.6 <a>三角锥型 <a>不等性sp3
第3题
A.在碱性溶液中与钴盐反应,生成紫堇色产物
B.在酸性溶液中硫酸铜试液反应,生成蓝紫色配合物
C.与硝酸汞试液反应,生成白色沉淀
D.在碱性溶液中与过量硝酸银试液反应,生成白色沉淀
E.在酸性溶液中与亚硝酸钠试液反应,生成重氮盐
第5题
已知
(A)
(B) 在标准状态时,反应 是自发进行的
是自发进行的
(C) 在酸性溶液中能发生歧化反应
(D) Fe与稀酸反应生成Fe2+和H2
第6题
A.MnO2能使KMnO4溶液保持稳定
B.Mn2+能催化KMnO4溶液的分解
C.用KMnO4溶液滴定Fe2+时,最适宜在盐酸介质中进行
D.用KMnO4溶液滴定H2C2O4时,开始时不能加热,否则草酸会分解
第8题
根据文中Mn的拉蒂麦尔图解释:

第9题


已知c(
第10题
A. 在稀溶液中能全部电离出 H+ 的盐酸、硫酸和硝酸
B. 在稀溶液中能全部电离出弱酸,如氢硫酸和腐植酸
C.强碱弱酸生成的盐类,如 Na3CO 3、NaPO 4、醋酸钠。
第11题
A.1:2
B.1:4
C.1:1
D.2:1