 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在铵盐存在下,利用氨水沉淀Fe3+,若铵盐浓度固定,增大氨的浓度,Fe(OH)3沉淀对Ca2+、Mg2+、Zn2+、Ni2+等四种离子
A.都增加
B.都减少
C.Zn2+、Ni2+增加,而Ca2+、Mg2+减少
D.Ca2+、Mg2+增加,而Zn2+、Ni2+减少
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.都增加
B.都减少
C.Zn2+、Ni2+增加,而Ca2+、Mg2+减少
D.Ca2+、Mg2+增加,而Zn2+、Ni2+减少
 答案
答案
 更多“在铵盐存在下,利用氨水沉淀Fe3+,若铵盐浓度固定,增大氨的浓度,Fe(OH)3沉淀对Ca2+、Mg2+、Zn2+、Ni2+等四种离子”相关的问题
更多“在铵盐存在下,利用氨水沉淀Fe3+,若铵盐浓度固定,增大氨的浓度,Fe(OH)3沉淀对Ca2+、Mg2+、Zn2+、Ni2+等四种离子”相关的问题
第1题
A、都增加
B、都减少
C、Zn2+、Ni2+增加,而Ca2+、Mg2+减少
D、Ca2+、Mg2+增加,而Zn2+、Ni2+减少
第4题
以氨水沉淀Fe3+时,溶液中含有Ca2+、Zn2+,当固定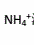 浓度、增大NH3浓度时,______的吸附量增大,______的吸附量减小。
浓度、增大NH3浓度时,______的吸附量增大,______的吸附量减小。
第5题
A.用氨气做喷泉实验,都会形成红色喷泉
B.所有铵盐都易溶于水,不是所有铵盐中的氮均呈-3价
C.氯化铝溶液中滴入过量的氨水:Al3++4OH-AlO2-+2H2O
D.NH4Cl和NaCl的固体混合物可用升华法分离
第7题
为分析硅酸盐中铁、铝、钛含量,称取试样0.6250g。除去SiO2后,用氨水沉淀铁、铝、钛为氢氧化物沉淀。沉淀灼烧为氧化物后重0.4165g。再将沉淀用K2S2O7熔融,浸取液定容于100mL容量瓶中。移取25.00mL试液通过锌汞还原器,含Fe2+和Ti3+的已还原液用含Fe3+的溶液承接,Fe3+被流入的Ti3+还原为Fe2+。然后用浓度为0.01390mol·L-1的K2Cr2O7标准溶液滴定,用去9.94mL。另取等量试液,用SnCl2将Fe3+还原为Fe2+,再用上述K2Cr2O7标准溶液滴定,用去8.82mL。计算试样中Fe2O3、Al2O3和TiO2的含量。[M(Fe2O3)=159.7g·mol-1,M(TiO2)=79.84g·mol-1,M(Al2O3)=102.0g·mol-1]
第8题
| (10分)金属氢氧化物在酸中溶解度不同,因此可以利用这一性质, 控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(s,mol·L-1)见图。
(1)pH=3时溶液中铜元素的主要存在形式是:____(写化学式) (2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH为____(填字母) A、<1 B、4左右 C、>6 (3)在Ni(NO3)2溶液中含有少量的Co2+杂质,____(能、不能)通过调节溶液pH的方法来除去,理由是____ (4)要使氢氧化铜沉淀溶解,除了加入酸之外,还可以 (5)已知一些难溶物的溶度积常数如下表。
 A、NaOH B、FeS C、Na2S |
第10题
已知Fe(OH)3的Ksp=3×10-39,若c(Fe3+)=0.010mol/L,则Fe(OH)3析出和沉淀完全的酸度条件为多少?