 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某课外兴趣小组欲在实验室里制备少量乙酸乙酯,该小组的同学设计了以下四个制取乙酸乙酯的装置,其中正确的是()。
A.
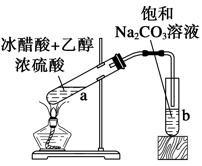
B.
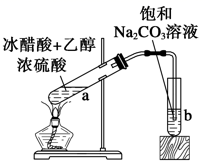
C.
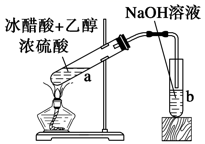
D.
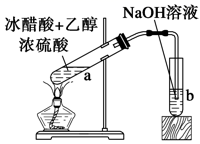
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.

B.

C.

D.

 答案
答案
 更多“某课外兴趣小组欲在实验室里制备少量乙酸乙酯,该小组的同学设计了以下四个制取乙酸乙酯的装置,其中正确的是()。”相关的问题
更多“某课外兴趣小组欲在实验室里制备少量乙酸乙酯,该小组的同学设计了以下四个制取乙酸乙酯的装置,其中正确的是()。”相关的问题
第1题
实验室里可用甲醇等有关物质制备HCHO,关于甲醇和甲醛的沸点和水溶性见下表: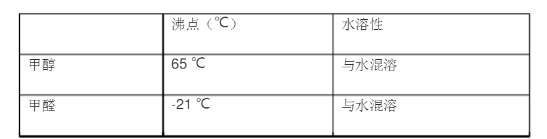 某校化学兴趣小组的甲、乙两位同学,在研究性学习中,运用以上信息和已有知识分别设计了二套实验室制取HCHO装置,如图甲和乙。
某校化学兴趣小组的甲、乙两位同学,在研究性学习中,运用以上信息和已有知识分别设计了二套实验室制取HCHO装置,如图甲和乙。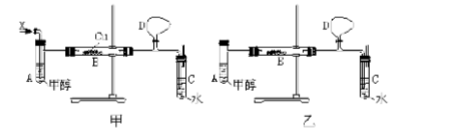
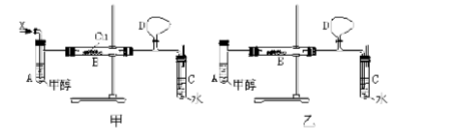 据此请你回答下列问题:
据此请你回答下列问题:
(1)若按甲装置进行实验,则通入A试管的X应是();B中反应的化学方程式是()。
(2)若按乙装置进行实验,则B管中应装入()。
(3)当实验完成时,若在C中滴加适量银氨溶液,并用水浴将C加热,发生反应的化学方程式是()。
(4)在反应过程中,甲、乙两种装置中都需直接加热的仪器是()(填A、B、C)。
(5)实验开始时,先打开气球D的开关,直至实验结束。气球D的作用是()。
(6)从生成甲醛的产量来看,你认为两套装置中较好的是()(填“甲”或“乙”)。
第3题
| 某化学兴趣小组在实验室利用氯气与石灰乳【Ca(OH)2】制取漂白粉. 已知2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O 该兴趣小组设计了下列实验装置,进行如下实验:
请回答下列问题: (1)实验室用甲装置用于制备氯气,其反应的化学方程式是______; (2)工业上电解饱和食盐水来制备氯气,其化学方程式是______; (3)乙装置的作用是______,丁装置的作用是______. (4)该兴趣小组用足量的浓盐酸与8.7g MnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2______g.但小组成员发现,实际上产物中Ca(ClO)2的质量明显小于理论值.为了探究其原因,小组成员查阅了相关资料得到:氯气和碱的反应为放热反应;温度较高时,氯气和碱还能发生如下反应:6Cl2+6Ca(OH)2 (5)为了提高Ca(ClO)2的产率,可对丙装置作适当改进.请你给出一种改进方法:______. |
第4题
| 某化学兴趣小组,向HCl 和CuCl2的混合溶液中,加入氢氧化钠溶液,实验结束后, 对所得“蓝色溶液”进一步探究。 【提出问题】 反应后的溶液中含有哪些溶质呢? 【猜想与假设】 甲同学猜想:溶液中溶质为CuCl2、NaCl 。 乙同学猜想:溶液中溶质只含有CuCl2。 【表达与交流】 (1) 甲同学猜想的理由是____________________________________________ ; 【反思与评价】 (2) 请对乙同学的猜想做出评价______________________________________ ; (3) 乙同学为了验证自己的猜想,取少量蓝色溶液于试管中,加入了氢氧化钠溶液,看到蓝 色沉淀,他认为自己的猜想是正确的。请对乙同学的实验设计做出评价______________ ; 【解释与结论】 (4) 若通过实验证明甲同学的猜想是错误的,则蓝色溶液中的溶质的化学式应该是_____ ; 【归纳与总结】 (5) 在探究化学反应后溶液中溶质成分时,需要考虑的是____________________________ 。 |
第5题
A、将SnCl2溶于碳酸钠溶液中,并加入少量锡粒
B、将SnCl2溶于新煮沸并冷却了的纯水中
C、将SnCl2溶于硫酸中,并加入少许锌粉
D、将SnCl2溶于盐酸中,并加入少量锡粒
第6题
| 某兴趣小组利用下图所示装置进行二氧化碳的制取与部分性质实验,请回答下列问题:
(1)关闭E打开C,从长颈漏斗A加入液体与锥形瓶B中固体接触,即有二氧化碳产生.观察到D中的蜡烛慢慢熄灭,说明二氧化碳具有______的性质,写出实验室制取二氧化碳的化学方程式______ (2)关闭C打开E,则观察到G中蜡烛燃烧得更旺,说明有氧气生成. [查阅资料]二氧化碳能与过氧化钠(Na2O2)反应生成碳酸钠与氧气 [实验探究]要检验反应后F中的固体物质含有碳酸钠,可取少量反应后F中固体物质于试管中,滴入______,观察到有气泡产生;用蘸有澄清石灰水的玻璃片放在试管口,观察到______,写出气体使石灰水变浑浊的化学反应方程式______; [实验结论]反应后F的固体物质含有碳酸根离子.写出二氧化碳与过氧化钠反应的化学方程式______; [拓展联系]利用虚线框内装置还可用于实验室制备氧气,该反应的化学方程式为:______. |
第7题
氯化镁是重要的无机材料,在常温下易吸湿,可溶于水和乙醇。某兴趣小组以海水为原料制备无水氯化镁。
实验一制备MgCl2·6H2O晶体
以海水为原料,对其进行一系列处理,得到晶体。
(1)除去海水中不溶性杂质常用的实验操作是()(填名称)。
(2)从氯化镁溶液中析出MgCl2·6H2O晶体的结晶方法是()(填“降温结晶”或“蒸发结晶”)。
实验二样品中MgCl2·6H2O晶体含量测定
准确称取实验一制得的MgCl2·6H2O晶体ag于锥形瓶中,加去离子水溶解,依次加入一定量三乙醇胺、NH3-NH4Cl缓冲溶液,摇匀,滴入铬黑T指示剂,用0.02000mol·L-1EDTA(用H2Y2-表示)标准溶液滴定至终点,消耗EDTA溶液的体积VmL。
已知:①0.02000mol·L-1EDTA标准溶液pH约为5,指示剂铬黑T使用的适宜pH范围为8~11,NH3-NH4Cl缓冲溶液pH约为10。
②滴定原理: Mg2++H2Y2-=MgY2-+2H+。
(3)使用的滴定管是()(填“甲”或“乙”)。
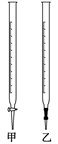 (4)NH3-NH4Cl缓冲溶液的作用是()。
(4)NH3-NH4Cl缓冲溶液的作用是()。
(5)样品中MgCl2·6H2O的质量分数为()。
实验三制备无水氯化镁
利用如图实验装置(夹持和加热装置省略),准确称取一定质量MgCl2·6H2O晶体在HCl气流中小心加热。
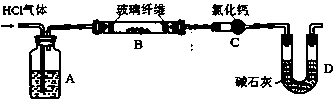 (6)A装置的作用是()。
(6)A装置的作用是()。
(7)某同学在实验前后测得玻璃管B减重m1g,干燥管C增重m2g,m1>m2,其可能的原因是()(用化学方程式表示)。
第8题
铝氢化钠(NaAlH4)是有机合成的一种重要还原剂。一般的制备方法是将力AlC13溶于有机溶剂,再把所得溶液滴加到NaH粉末上,可制得铝氢化钠。实验要求和装置如下,回答下列问题:
1)制取铝氢化钠要在非水溶液中进行,主要原因是()(用化学方程式表示)。用下列装置制取少量铝氢化钠(含副产物处理)较为合理的是()。 2)对于原料ALCL3的制取,某兴趣小组设计了如下装置:
2)对于原料ALCL3的制取,某兴趣小组设计了如下装置: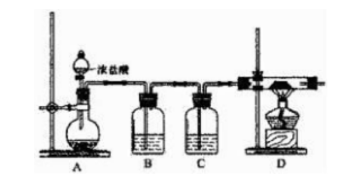 ①连接好装置后,应进行的第一步操作是();为保证产物的纯净,应待D中()(填现象)再加热酒精灯。
①连接好装置后,应进行的第一步操作是();为保证产物的纯净,应待D中()(填现象)再加热酒精灯。
②B装置中盛装饱和NaCl溶液,实验开始后B中产生的现象是(),选择NaCl饱和溶液的理由是()。
③C装置的作用是();若无C装置,试预测实验后D中生成物除A1C13外可能还含有()。(填化学式)。
④上述装置存在的明显缺陷是()。
第9题
某废催化剂主要成分有SiO2、ZnO、ZnS和CuS。某化学兴趣小组拟用该废催化剂为原料,制备硫酸锌和硫酸铜晶体。采用的实验方案如下,下列说法正确的是()。 已知:ZnS与稀硫酸发生反应且化合价不变,CuS既不溶于稀硫酸也不和稀硫酸反应
A.第一次浸出可以在烧杯中进行
B.第二次浸出时发生反应为CuS+H2O2+H2SO4=CuSO4+S+2H2O
C.滤渣2中只有二氧化硅
D.获得硫酸锌和硫酸铜晶体采用蒸发结晶的方式
第11题
| (1)(3分)规范的实验操作是实验成功的前提,请回答: ①用漏斗过滤时,注意液面始终要____。 ②点燃氢气前应先____。 ③玻璃管插入带孔橡皮塞,先把玻璃管的一端____,然后稍稍用力转动插入。 (2)(5分)某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验。 甲同学选用如右图所示的装置制取氧气。
①写出仪器B的名称:_______。 ②甲同学应选取的试剂是Mn02和_________(填化学式), Mn02固体在该反应中起________作用。 ③除用排水法外,甲同学还可选择______法收集氧气。 ④加入药品前,甲同学先向仪器A中加入水,然后将导管放人水槽中,并打开仪器A的活塞,观察导管口是否有连续的气泡出现。该实验操作的目的是____________。 |