 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在含有1.000 mol·L-1硫酸锌与1.000mol·L-1酸镉的1.0mol·L-1的硫酸介质中,进行电解实验。(E(zn2+/zn)=-0.763
在含有1.000 mol·L-1硫酸锌与1.000mol·L-1酸镉的1.0mol·L-1的硫酸介质中,进行电解实验。(E (zn2+/zn)=-0.763 V,E
(zn2+/zn)=-0.763 V,E (Cd2+/Cd)=-0.403V)试计算:
(Cd2+/Cd)=-0.403V)试计算:
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在含有1.000 mol·L-1硫酸锌与1.000mol·L-1酸镉的1.0mol·L-1的硫酸介质中,进行电解实验。(E (zn2+/zn)=-0.763 V,E
(zn2+/zn)=-0.763 V,E (Cd2+/Cd)=-0.403V)试计算:
(Cd2+/Cd)=-0.403V)试计算:
 答案
答案
 更多“在含有1.000 mol·L-1硫酸锌与1.000mol·L-1酸镉的1.0mol·L-1的硫酸介质中,进行电解实验。(E(zn2+/zn)=-0.763”相关的问题
更多“在含有1.000 mol·L-1硫酸锌与1.000mol·L-1酸镉的1.0mol·L-1的硫酸介质中,进行电解实验。(E(zn2+/zn)=-0.763”相关的问题
第1题
已知E (Ag+/Ag)=0.800 V,E
(Ag+/Ag)=0.800 V,E (Cu2+/Cu)=0.337V。在25℃时,在含有1.000×10-2mol·L-1的Ag+和1.000 mol·L-1的Cu2+离子的硫酸盐溶液中,首先在阴极上还原的是______,开始析出时的阴极电位为______。
(Cu2+/Cu)=0.337V。在25℃时,在含有1.000×10-2mol·L-1的Ag+和1.000 mol·L-1的Cu2+离子的硫酸盐溶液中,首先在阴极上还原的是______,开始析出时的阴极电位为______。
第2题
电解1.000×10-2mol·L-1硫酸锌溶液,当介质为0.50mol·L-1硫酸溶液时,锌是否能在铂电极上析出?如果介质[H<sup>+</sup>]=10-5mol·L-1时,锌是否能析出?(在锌电极上,ηH2=-0.70V;E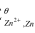 (zn2+/zn)=-0.763V)
(zn2+/zn)=-0.763V)
第3题
在0.10 mol?L-1HCIO4溶液中,以铂电极为阴极,电解1.000×10-2 mol?L-1 Cu2+和1.000×10-2mol?L-1Sn2+的混合溶液。试指出在阴极上离子的析出顺序。(已知
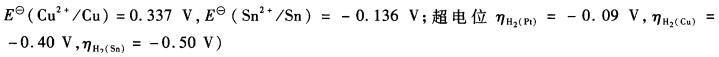
第4题
含有cHA=cHB=0.10 mol·L-1的混合溶液(pKHA=5.0,pKHB=9.0)的pH值应为()。
A.1.00
B.3.00
C.4.00
D.7.00
第5题
一电导池充以1.000×10-3mol·L-1的HCl溶液,25℃时测得其电阻为468 Ω,充以1.000×10-3mol·L-1的NaCl溶液,25℃时测得其电阻为1 580 Ω,充以1.000×10-3mol·L-1的NaNO3溶液,25℃时测得其电阻为1 650 Ω。如果NaNO3的摩尔电导率为121 S·cm2·mol-1,不考虑摩尔电导率随浓度的变化时,试计算:
第6题
在0.1 mol?L-1KCl溶液中,1.00×10-41mol?L-1的Cd2+与不同浓度的A-所形成的配离子,其可逆极谱波的半波电位值如下:

第7题
第8题
在100 mL 0.10 mol·L-1HCl中,用控制电位库仑法于一0.65 V(vs.SCE)测定0.045 8 mmol·L-1苦味酸。与电解池串联的库仑计测得其电量为75.4 C。计算此还原反应中的电子转移数n,并写出电极反应。
第9题
在0.1 mol·L-1KCl溶液中,1.00×10-4mol·L-1的Cd2+与不同浓度的A-所形成的配离子,其可逆极谱波的半波电位值如下:
cA-/(mmol·L-1) | O.00 | 1.00 | 3.00 | 10.00 | 30.00 |
E1/2/V | -0.586 | -O.719 | -0.743 | -0.778 | -0.805 |
电极反应为Cd2++2e-+Hg Cd(Hg),计算该配合物的化学式及稳定常数。
Cd(Hg),计算该配合物的化学式及稳定常数。
第10题
在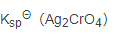 )=0.10mol·L-1的溶液中,Ag2CrO4的溶解度S/mol·L-1等于:
)=0.10mol·L-1的溶液中,Ag2CrO4的溶解度S/mol·L-1等于:
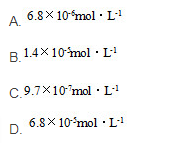
第11题
用库仑法测定溶液中的As(Ⅲ),电解质为0.1 mol·L-1的H2SO4和0.2 mol·L-1的KBr,在_______极上产生滴定剂,电极反应是________。