 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
N2O5的热分解反应在不同温度下的速率常数如下,求:(1)Arrhenius公式中的Ea和A;(2)该反应在323.15K
N2O5的热分解反应在不同温度下的速率常数如下,求:(1)Arrhenius公式中的Ea和A;(2)该反应在323.15K温度下的△G≠、△H≠、△S≠。
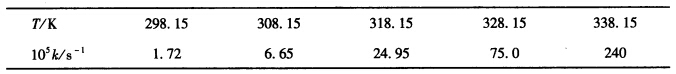
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
N2O5的热分解反应在不同温度下的速率常数如下,求:(1)Arrhenius公式中的Ea和A;(2)该反应在323.15K温度下的△G≠、△H≠、△S≠。

 答案
答案
 更多“N2O5的热分解反应在不同温度下的速率常数如下,求:(1)Arrhenius公式中的Ea和A;(2)该反应在323.15K”相关的问题
更多“N2O5的热分解反应在不同温度下的速率常数如下,求:(1)Arrhenius公式中的Ea和A;(2)该反应在323.15K”相关的问题
第1题
某顺式偶氮烷烃在乙醇溶液中不稳定,通过计量其分解放出的N2(g)来计算其分解的速率常数k值,不同温度下测定的一系列k值如下:
| T/K | 248 | 252 | 256 | 260 | 264 |
| k/(10-4s-1) | 1.22 | 2.31 | 4.39 | 8.50 | 14.3 |
试计算该反应在298K时的实验活化能Ea、活化焓


第2题
某分解反应在10℃的速率常数为4.5×10-3s-1,活化能为58kJ·mol-1,求在什么温度下,该反应的速率常数为10×10-4s-1?
第3题
已知298.15K、100kPa下,N2O5(g)、NO2(g)和O2(g)的标准摩尔生成热分别为2.51kJ/mol、33.85kJ/mol和0kJ/mol,标准摩尔熵分别为342.40J/(mol·K)、240.57J/(mol·K)和205.14J/(mol·K)。求反应
第4题
气相反应动力学分析
N2O5在45℃发生如下的分解反应:
2N2O5→2N2O4+O2
反应是在恒容反应器中进行,实验测得的N2O5的分压与时间的关系列于下表。试根据这些数据计算反应级数和反应速率常数。
t(min) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
pN2O5(Pa) | 32933 | 24666 | 18666 | 13999 | 10400 | 7733 | 5867 | 4400 | 3200 | 1867 |
第5题
反应:2N2O5(g)====4NO2(g)+O2(g)
起始时N2O5(g)浓度为1.15mol·dm-3,100s后测得N2O5(g)浓度为1.0mol·dm-3,则反应在100s内的平均速率为多少?
第6题
经测定过氧化二苯甲酰在不同温度下于甲苯中的分解速率常数为
温度/℃ | kd×104/min-1 |
50 60 70 80 | 1.57 5.48 23.2 85.0 |
试计算其在50℃及60℃时的半衰期t1/2(h)及分解活化能Ed。
第7题
在活塞流反应器中,乙烷热裂解制乙烯,反应式为:
C2H6→C2H4+H2
A R S
反应在(0.14Mpa,1173K)下通入水蒸气进行裂解,水蒸气与乙烷的摩尔比为0.5:1,乙烷进料为每小时20t,其转化率为60%。假设该反应为一级不可逆反应,并忽略其他副反应,试计算所需的反应体积。已知:反应速率常数为k=1.535×104exp(-70200/RT)(s-1)。
第8题
碘化氢分解反应:2HI→H2+I2,已知临界能Ec=183.92kJ/mol,HI的分子直径d=3.5×10-10m,摩尔质量为127.9g/mol。试由碰撞理论计算在不同温度下HI分解的速率常数k并和下列实验数据相比较。

第9题
已知反应A→P的动力学方程为(-rA)=kcA。在给定温度下,k=0.2h-1。进料A初始组成为A的饱和水溶液,其cA0=1mol/L,反应在CSTR中进行时,求生产产品P为100mol/h的最优反应体积、最优进料速率和最优转化率。又若在PFR中进行该反应时,求最优反应体积,最优进料速率和最优转化率。
第10题
一气相热分解反应A→P+Q的反应速率方程为
r=kpA式中r的单位为mol·m-3·min-1。
该反应在内径为0.0127m,长3.0m的管式反应器内进行。反应物料流量(标准状态,273K,101.3kPa)为1.50×10-4m3/min。在反应过程中温度恒定,压力保持101.3kPa,在反应温度下的反应速率常数为0.465mol/(kPa·m3·min),反应物料只含有A,不含其他组分,试求反应器出口处的A的转化率。
第11题
碘化氢分解反应:2HI→H2+I2,已知临界能Ec=183.92kJ/mol,HI的分子直径d=3.5×10-10m,摩尔质量为127.9g/mol。试由碰撞理论计算在不同温度下HI分解的速率常数k并和下列实验数据相比较。
| T(K) k[m3/(mol·s)] | 556 3.52×10-10 | 666 2.20×10-7 | 781 3.95×10-5 |