 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K下测得0.005mol·L-1NaCl溶液的电阻为2.619×l03Ω,0.1mol·L-1KCl溶液则为122.6Ω,已知298K下0.1mol·L-1KCl
298K下测得0.005mol·L-1NaCl溶液的电阻为2.619×l03Ω,0.1mol·L-1KCl溶液则为122.6Ω,已知298K下0.1mol·L-1KCl溶液的电导率为0.01289S·cm-1,计算NaCl溶液的摩尔电导率。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K下测得0.005mol·L-1NaCl溶液的电阻为2.619×l03Ω,0.1mol·L-1KCl溶液则为122.6Ω,已知298K下0.1mol·L-1KCl溶液的电导率为0.01289S·cm-1,计算NaCl溶液的摩尔电导率。
 答案
答案
 更多“298K下测得0.005mol·L-1NaCl溶液的电阻为2.619×l03Ω,0.1mol·L-1KCl溶液则为122.6Ω,已知298K下0.1mol·L-1KCl”相关的问题
更多“298K下测得0.005mol·L-1NaCl溶液的电阻为2.619×l03Ω,0.1mol·L-1KCl溶液则为122.6Ω,已知298K下0.1mol·L-1KCl”相关的问题
第1题
298K时测得不同浓度c下氢化肉桂酸水溶液的表面张力σ的数据如下表所示:
 求浓度为0.0041kg/kg及0.0050kg/kg时溶液表面吸附量
求浓度为0.0041kg/kg及0.0050kg/kg时溶液表面吸附量
 。
。
第2题
298K时测得不同浓度c下氢化肉桂酸水溶液的表面张力σ的数据如下表所示:
| c/(kg/kg) σ×103/(N/m) | 0.0035 56.0 | 0.0040 54.0 | 0.0045 52.0 |
第3题
298K时在滴汞电极进行Mn++ne=M的可逆反应,在不同电位下测得的电流如下表所示。(1)用作图法求出E1/2和n。(2)当Mn+的浓度为2.98×10-3mol·L-1时,汞的流速为3.299 mg·s-1,汞滴从开始到滴下的时问为2.47s,计算Mn+的扩散系数。
-E/V vs SCE | 0.97 | 0.98 | 0.99 | 1.01 | 1.02 | 1.03 | 1.04 | 1.05 |
overline{I}/μA | 2.134 | 4.255 | 7.718 | 17.100 | 20.644 | 22.831 | 25.000 | 25.000 |
第4题
第5题
电池Mo(S)|MoS2(S)|H2S(100kPa)|KCl(0.01mol/kg)|HCl(0.01mol/kg)|H2(100kPa)|Pt,测得其在不同温度下的电池电动势数据为 T/K 288 298 308 E/V 0.4148 0.4119 0.4087 (1)写出电极反应和电池反应; (2)由题给数据推导出电池反应的平衡常数与温度的关系式,并计算△rHm; (3)用电化学方法计算298K时电池反应的△rSm,将其与热力学方法计算所得结果相比较可得出什么结论?298K时,物质的规定熵数据为 物质 H(g)H2S(g) Mo(s) MoS2(s) Sm/[J/(K.mol)] 130.6 205.6 28.58 62.59
第6题
在298K时,测得某聚合物溶液在不同浓度时的相对黏度如下:
| c/(g·100dm-3) | 0.152 | 0.271 | 0.541 |
| ηr | 1.226 | 1.425 | 1.983 |
求此聚合物的特性黏度[η]。
第8题
在弹式量热计中燃烧氮化铌反应为
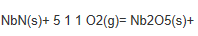
 在298K时测得热力学能的变化为-712.97kJ·mol-1,求此反应的焓变。
在298K时测得热力学能的变化为-712.97kJ·mol-1,求此反应的焓变。
第9题
由标准氢电极(SHE)(下图左边的参考电极)和已浸入锌离子溶液的锌棒组成的自发电池在298K时测得电动势为-0.789V。锌离子的活度为多少?

第10题
在298K时,将含有1mg蛋白质的水溶液铺在质量分数为0.05的(NH4)2SO4溶液表面,当溶液表面积为0.1m2时,测得其表面压π=6.0×10-4N·m-1。试计算该蛋白质的摩尔质量。
第11题
在298K时,将含有Sn(ClO4)2和Pb(ClO4)2的某溶液与过量的粉末状Sn-Pb合金一起振荡后,测得溶液中平衡浓度之比[Pb2+]/[Sn2+]为0.46。已知
 =-0.126V,计算
=-0.126V,计算
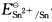 值。
值。