 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
其他物质均处于标准态,增大溶液H+浓度,下列电极电势增大最多的是( )。
A.φ(O2/H2O)
B.
C.
D.φ(Zn2+/Zn)
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.φ(O2/H2O)
B.
C.
D.φ(Zn2+/Zn)
 答案
答案
 更多“其他物质均处于标准态,增大溶液H+浓度,下列电极电势增大最多的是()。 A.φ(O2/H2O) B. C. D.φ(Zn2+/Zn)”相关的问题
更多“其他物质均处于标准态,增大溶液H+浓度,下列电极电势增大最多的是()。 A.φ(O2/H2O) B. C. D.φ(Zn2+/Zn)”相关的问题
第2题
当各物质均处于标准态时,下列反应能正向进行的是()。
A.2Cl-+Br2=2Br-+Cl2
B.2Fe3++2C1-=Cl2+2Fe2+
C.2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2
D.6Fe3++2Cr3++7H2O=6Fe2++Cr2O72-+14H+
第4题
当下列各酸水溶液中的H+浓度(单位:mol/L)相等时,哪一种溶液中物质的量浓度最大?( )
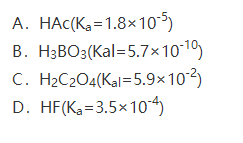
第5题
在1 L 0.2 mol·L-1NaOH溶液中通入标准态下的SQ3 4.48 L,完全反应后,下述关系式中正确的是()。
A.[Na+]+[H+]=[HSO3-]+2[SO32-]+[OH-]
B.[Na+]+[H+]=[HSO3-]+[SO32-]+[OH-]
C.[Na+]>[HSO3-]>[H+]=[SO32->[OH-]
D.[Na+]>[HSO3-]>[OH-]>[SO32-]>[H+]
第6题
当下列各种酸的水溶液中H+浓度(单位为mol·dm-3)相等时,何种溶液中原物质的量浓度为最大?
A.HCOOH(ka=1.8×10-4) B.H3BO3(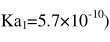 )
)
C.H2C2O4(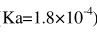 ) D.HF(Ka=3.5×10-4)
) D.HF(Ka=3.5×10-4)
E.HIO3(Ka=1.7×10-1)
第7题
16. 稀溶液的电导比例于离子浓度,因而产生离子的反应可通过电导测定来确定反应的进程。叔戊基碘在乙醇水溶液中的水解反应
t-C5H11I+H2O→t-C5H11OH+H++I-
为一级反应。现此反应在电导池中进行,由于反应不断产生H+和I-,因而溶液电导G不断地随时间t而增大。若G0,G和G∞分别为t=0,t=t和t=∞时的电导,c0和c分别为t=0,t=t时t-C5H11I的浓度。试证:

第9题
A.错误
B.正确
第10题
当一个溶液用不同浓度标志时,对于某一组分B,下列哪种表述是正确的?
(A) αB不变 (B) γB不变 (C) 标准态相同 (D) 化学势不变
第11题
25℃时氯气溶于水(溶解度为0.090 moldm-3)发生下列反应: Cl2(g)+H2O(l) = Cl-(aq)+H+(aq)+HClO(aq) 其标准平衡常数KΘ=4.2×10-4。求在此温度下饱和氯水溶液中Cl-、H+的浓度是多少?