 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
由下列元素电势图可确定298.15 K时给定反应的平衡常数为(). A.3.8×10-66B.1.3×10-54C.7
由下列元素电势图可确定298.15 K时给定反应的平衡常数为().
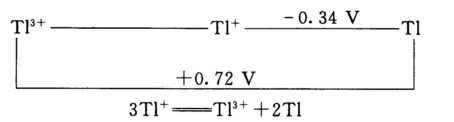
A.3.8×10-66
B.1.3×10-54
C.7.0×1030
D.2.1×1017
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
由下列元素电势图可确定298.15 K时给定反应的平衡常数为().

A.3.8×10-66
B.1.3×10-54
C.7.0×1030
D.2.1×1017
 答案
答案
 更多“由下列元素电势图可确定298.15 K时给定反应的平衡常数为(). A.3.8×10-66B.1.3×10-54C.7”相关的问题
更多“由下列元素电势图可确定298.15 K时给定反应的平衡常数为(). A.3.8×10-66B.1.3×10-54C.7”相关的问题
第1题
甘油三油酸脂(相对分子质量884)在人体内可发生如下代谢反应: C57H104O6(s)+80O2(g)===57CO2(g)+52H2O(1) △fHmθ(298.15 K)=一3.35×104kJ.mol-1 计算:(1)1 g这种脂肪代谢时可放出多少热量? (2)△fHmθ(C57H104O6,S,298.15 K)=? 已知: O2(g) CO2(g) H2O(1) △fHmθ(298.15 K)/(kJ.mol-1) 0 —393.5 —285.8
第2题
说明下列符号的意义:S、




第3题
比较下列物质SΘm(298.15 K)值的大小。 (a)Ag(s) (b)AgCl(s) (c)Cu(s) (d)C6H6(l) (e)C6H6(g)
第4题
有两支试管:在A试管中,滴加2滴酸化的KMnO4溶液于过量的KI溶液中;在B试管中滴加2滴KI溶液于过量酸化的KMnO4中。根据上述实验及下面的元素电势图,确定两支试管中发生的现象,写出有关的离子反应式。


第5题
第6题
写出由元素化合生成1 mol CH4(g)的化学方程式,由下列方程和293 K 时的△rHmθ值计算CH4的生成热。 H2(g)+
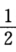 O2(g)→H2O(1) △rHmθ=一286.1 kJ.mol-1 C(s)+O2(g)→CO2(g) △rHmθ=一394.9 kJ.mol-1 CH4(g)+2O2(g)→CO2(g)+2H2O(1) △rHmθ=一882.0 kJ.mol-1
O2(g)→H2O(1) △rHmθ=一286.1 kJ.mol-1 C(s)+O2(g)→CO2(g) △rHmθ=一394.9 kJ.mol-1 CH4(g)+2O2(g)→CO2(g)+2H2O(1) △rHmθ=一882.0 kJ.mol-1
第8题
已知: C2H2(g) O2(g) CO2(g) H2O(1) △fHmθ(298.15 K)/(kJ.mol-1) 226.73 0 —393.5 —285.8 计算C2H2的燃烧焓。
第10题
A.M2+不能发生歧化反应
B.M2+是强氧化剂
C.M是强还原剂
D.M4+ 与M 反应生成M2+