 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算下列甲醇(1)一水(2)系统的组分逸度。 (1)p=101325Pa,T=81.48℃,y1=0.582的气相; (2)p=101325
计算下列甲醇(1)一水(2)系统的组分逸度。 (1)p=101325Pa,T=81.48℃,y1=0.582的气相; (2)p=101325Pa,T=81.48℃,x1=0.2的液相。已知液相符合Wilson方程,其模型参数是
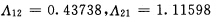 。
。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算下列甲醇(1)一水(2)系统的组分逸度。 (1)p=101325Pa,T=81.48℃,y1=0.582的气相; (2)p=101325Pa,T=81.48℃,x1=0.2的液相。已知液相符合Wilson方程,其模型参数是
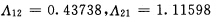 。
。
 答案
答案
 更多“计算下列甲醇(1)一水(2)系统的组分逸度。 (1)p=101325Pa,T=81.48℃,y1=0.582的气相; (2)p=101325”相关的问题
更多“计算下列甲醇(1)一水(2)系统的组分逸度。 (1)p=101325Pa,T=81.48℃,y1=0.582的气相; (2)p=101325”相关的问题
第1题
计算甲醇(1)一水(2)系统的露点(假设气相是理想气体,可用软件计算)。(1)p=101325Pa,y1=0.582(实验值T=81.48℃,x1=0.2);(2)T=67.83℃,y1=0.914(实验值p=101325Pa,x1=0.8)。 已知:Wilson能量参数λ12—λ11=1085.13J/mol和λ21一λ22=1631.04 J/mol。
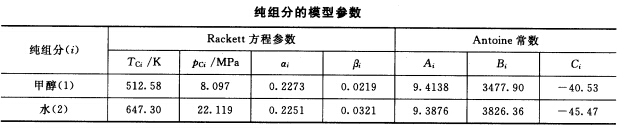
第2题
测定了异丁醛(1)一水(2)系统在30℃时的液液平衡数据是x1α=0.8931,x1=0.0150。由此计算van Laar常数。已知30℃时,p1s=28.58kPa,p2s=4.22 kPa。
第3题
某温度时在水、乙醚和甲醇的各种三元混合物中二液层的组成如下:
| 甲醇%(质量分数) | 0 | 10 | 20 | 30 | |
| 水% (质量分数) | 液层(1) | 93 | 82 | 70 | 45 |
| 液层(2) | 1 | 6 | 15 | 40 |
根据以上数据绘制三组分系统相图,并指出图中各区相态。
第4题
试计算下表所述精馏系统的最小回流比。已知进料中的液相率为0.4
组分 | αi | xiF | xiD |
1,正辛烷 | 1 | 0.34 | 0.0 |
2,正庚烷 | 2.27 | 0.33 | 0.01 |
3,正己烷 | 5.25 | 0.33 | 0.99 |
第5题
醋酸甲酯(1)和甲醇(2)}昆合物系的范拉尔常数(用ln表示)为A12=1.029,A21=0.946,在54℃时,纯组分的饱和蒸气压数据分别为

第6题
在环境温度为294.4K,压力为101.3kPa的条件下分离流率为24898kmol/h的甲醇一水混合液体。原料中含甲醇58.07%(摩尔分数),所得产品为含甲醇99.05%(摩尔分数)的富甲醇产品和含甲醇1.01%(摩尔分数)的废水。确定过程需要的最小功。根据VanLaar方程计算液相活度系数,
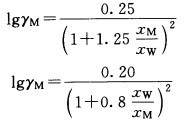 式中,M代表甲醇,W代表水。
式中,M代表甲醇,W代表水。
第7题
醋酸甲酯(1)和甲醇(2)混合物系的范拉尔常数(用ln表示)为A12=1.029,A21=0.946,在54℃时,纯组分的饱和蒸气压数据分别为P10=0.0903MPa,P20=0.066MPa。 试判断: (1)在54℃时有无恒沸物? (2)形成什么样的恒沸物?
第8题
在一水平面上有两根相互平行的固定导轨M1N1和M2N2,质量m1的物块P1穿在M1N1上,质量m2的物块P2穿在M2N2上,P1与P2间用一根不可伸长的轻绳连接,开始时绳处于松弛状态。今使P1获得沿导轨方向速度υ0,P2静止,如图所示,设系统处处无摩擦,P1运动一段时间后绳被拉直,其内产生拉力,同时使导轨与相应的物块间有力的作用,这些力的作用时间Δt非常短。试就下述两种情况,计算Δt刚结束时P1,P2运动速度u1,u2

(1)绳的作用不损耗系统动能;
(2)绳的作用使P1,P2沿绳长方向的速度相同。
第9题
第10题
组分A按下列反应发生分解:
A====B+C
该反应是在60℃下于液相中进行的。反应的平衡常数为2。组分A、B和C在60℃下的饱和蒸气压分别为607.95kPa、1013.25kPa和810.60kPa。液体A和液体C形成理想溶液。液体B与由(A+C)组成的溶液中互不相溶。假设其汽相为理想气体。试计算该系统在60℃下的汽相组成和平衡压力。
通用气体常数R=1.987cal·mol-1·K-1或8.315J·mol-1·K-1(1cal=4.184J)。
第11题