 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据实验测得1mol H2SO4溶于n1mol水中时,溶解热△isolH可用下式表示 式中a=7.473×104J;b=1
根据实验测得1mol H2SO4溶于n1mol水中时,溶解热△isolH可用下式表示
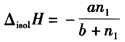 式中a=7.473×104J;b=1.798mol。试求: (1)积分溶解热,用1mol H2SO4溶于10mol水中。 (2)积分稀释热,在上述溶液中再加10mol水。
式中a=7.473×104J;b=1.798mol。试求: (1)积分溶解热,用1mol H2SO4溶于10mol水中。 (2)积分稀释热,在上述溶液中再加10mol水。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据实验测得1mol H2SO4溶于n1mol水中时,溶解热△isolH可用下式表示
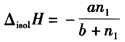 式中a=7.473×104J;b=1.798mol。试求: (1)积分溶解热,用1mol H2SO4溶于10mol水中。 (2)积分稀释热,在上述溶液中再加10mol水。
式中a=7.473×104J;b=1.798mol。试求: (1)积分溶解热,用1mol H2SO4溶于10mol水中。 (2)积分稀释热,在上述溶液中再加10mol水。
 答案
答案
 更多“根据实验测得1mol H2SO4溶于n1mol水中时,溶解热△isolH可用下式表示 式中a=7.473×104J;b=1”相关的问题
更多“根据实验测得1mol H2SO4溶于n1mol水中时,溶解热△isolH可用下式表示 式中a=7.473×104J;b=1”相关的问题
第1题
根据实验测得1molH2SO4溶于n1mol水中时,溶解热△isolH可用下式表示
式中a=7.473×104J;b=1.798mol。试求:
第3题
A.蛋白质原料用6~10mol,/L HCl于110℃~120℃水解12~24h
B.蛋白质原料用1mol/L H2SO4于110℃~120℃水解12~24h
C.此法水解迅速而彻底,产物全部为L-型氨基酸,无消旋作用
D.色氨酸全部被破坏,丝氨酸部分被破坏
第4题
Cd2+在1mol·L-1HCl溶液中于-0.640V显示一可逆的两电子还原波,测得0.500mmol·L-1Cd2+溶液极谱波在E1/2处的扩散电流为3.96μA,毛细管特性是v=2.50mg·s-1,t=3.02s。计算:
第5题
称取土壤样品6.00g,用pH=7的1mol·dm-3醋酸铵提取,离心,转移含钙的澄清液于100cm3容量瓶中,并稀释至刻度。取50.00cm3该溶液在25℃时用钙离子选择性电极和SCE电极测得电动势为20.0mV,加入0.0100mol·dm-3的标准钙溶液1.0cm3,测得电动势为32.0mV,电极实测斜率为29.0mV,计算土壤样品中Ca2+的质量分数。
第6题
设塑料的抗压强度近似服从正态分布,且相互独立.现有两种塑料,已知方差



第7题
有一黑色化合物(I),不溶于碱,加热时可溶于浓盐酸而放出气体(II)。将(I)与NaOH和KClO3共热,它就变成可溶于水的绿色化合物(III)。若将(III)酸化,则得到紫红色溶液(IV)和沉淀(I)。用Na2SO3溶液处理(IV)时,也可得到沉淀(I)。若用H2SO4酸化的Na2SO3溶液处理(Mn2+盐),则得到几近无色的溶液(V)。问(I), (II), (III), (IV)各为何物?
A(I) = MnO2, (II)= Cl2, (III)= MnO42-, (IV)= MnO4-;
B(I) = MnO2, (II)= Cl2, (III)= MnO4-, (IV)= MnO42-;
C(I) = MnO2, (II)= O2, (III)= MnO42-, (IV)= MnO4-;
D以上都不是
第8题
将金属镉溶于硝酸中配制成镉的标准溶液,使用228.8 nm的分析线测得原子吸光分析值如下:
 问:(1)是否符合比耳定律? (2)有一未知样品,测得其透光率为89.5%,求样品中镉的质量浓度。
问:(1)是否符合比耳定律? (2)有一未知样品,测得其透光率为89.5%,求样品中镉的质量浓度。
第9题
| 某无色溶液可能是由Na2CO3、NaOH、MgCl2、AlCl3、BaCl2、Fe2(SO4)3、(NH4)2SO4溶液中的两种或两种以上混合而成.取该溶液少许于试管,向其中加入H2SO4,有白色沉淀生成,继续加入H2SO4时沉淀又完全消失,整个实验过程中无气体产生,则原溶液是由______ 和______ 混合而成.实验过程中有关的离子反应方程式是______. |
第10题
A、(I)=NaMnO4,(II)=O2,(III)=NaMnO3;
B、(I)=NaNO3,(II)=O2,(III)=NaNO2;
C、(I)=NaClO3,(II)=O2,(III)=NaClO;
D、(I)=NaSO4,(II)=O2,(III)=NaSO3
第11题
用光切显微镜测得工件某表面在取样长度lri内各最高点和最低点的格数Ni(见表1.5-1),目镜测微计分度值i=0.6μm,试计算该表面的Rz值。
| 表1.5-1 工件取样长度内最高点和最低点的格数 | |||||
| lri | lr1 | lr2 | lr3 | lr4 | lr5 |
| 最高点N1/格 | 438 | 448 | 464 | 506 | 516 |
| 最低点N2/格 | 478 | 474 | 498 | 534 | 558 |