 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在c(Pb2+)=0.010 mol.dm-3和c(Mn2+)=0.0 1 0 mol.dm-3的溶液中,通入H2S气体达到饱和,若要使PbS沉
在c(Pb2+)=0.010 mol.dm-3和c(Mn2+)=0.0 1 0 mol.dm-3的溶液中,通入H2S气体达到饱和,若要使PbS沉淀完全而MnS不沉淀,问溶液的pH应控制在什么范围? (已知Kspθ(PbS)=8×10-28,Kspθ(MnS)=1.4×10-15,H2S:Ka1θ=1.3×10-7,Ka2θ=7.1×10-15)
 答案
答案





 大小相近,在PhI2、CaCO3两饱和水溶液中:
大小相近,在PhI2、CaCO3两饱和水溶液中: 的混合溶液中,逐滴加入含Pb2+的溶液,当PbCrO4和PbSO4共同沉淀时,溶液中
的混合溶液中,逐滴加入含Pb2+的溶液,当PbCrO4和PbSO4共同沉淀时,溶液中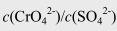 为( )
为( )




















