 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A、B、C、D四种物质的转化关系如图所示,它们均为初中化学中常见的物质,其中A是一种黑色氧化物,B物质的溶液呈蓝色.则X可能为()
A.H2S04
B.HCl
C.NaOH
D.Cu(OH)2
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)

A.H2S04
B.HCl
C.NaOH
D.Cu(OH)2
 答案
答案
 更多“A、B、C、D四种物质的转化关系如图所示,它们均为初中化学中常见的物质,其中A是一种黑色氧化物,B物质的溶液呈蓝”相关的问题
更多“A、B、C、D四种物质的转化关系如图所示,它们均为初中化学中常见的物质,其中A是一种黑色氧化物,B物质的溶液呈蓝”相关的问题
第2题
| 如图所示,NaOH、NaCl、Na2CO3、Na2SO4四种物质通过适当的反应,均可转化为X. (1)X的化学式为______. (2)写出有关的化学方程式: ①______②______ ③______④______ ⑤______⑥______ ⑦______⑧______.
|
第3题
| 体,C、D、E常温下均为气体,C的相对分子质量大于E。请回答:
(1) A的化学式____;D的化学式____。 (2)写出B向C转化的反应方程式____。 (3)E在生产生活中的用途____。(答一条即可) |
第4题
| 由H、O、Cu三种元素组成的初中常见物质间有如图所示的关系,其中A、B、C是单质,甲乙是化合物,图中“-”表示相连的物质俩俩之间可以发生反应,“→”表示由某一物质可制得另一物质,(部分反应物、生成物及反应条件略去),回答下列问题: (1)写出下列物质的化学式:C______,甲______; (2)写出A和B反应的化学方程式______.
|
第5题
| 已知草酸(H2C2O4)在浓硫酸的催化作用下,加热能分解产生三种化合物B、C、D,它们与其它物质间的转化关系如下图所示,其中E是由两种元素组成的化合物,其相对分子质量为160,X、Y、Z均为单质。试解答下列问题: |
|
| (1)写出有关物质的化学式: C _________;E_________;Y_________。 (2)写出有关反应的化学方程式: 反应①_______;反应③_________。 (3)说出单质Y的用途__________(一条即可)。 (4)反应④是Z和____________(填试剂的名称)的反应。 |
第7题
| 工业上用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,称为氯碱工业。 (1)若采用无隔膜法电解冷的食盐水时,Cl2会与NaOH充分接触,导致产物仅是NaClO和H2。无隔膜法电解冷的食盐水相应的离子方程式为____。 (2)氯碱工业耗能高,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①经精制的饱和NaCl溶液应从图中电解池的____(填写“左” 或“右”)池注入。 ②图中X是__________(填化学式);乙中右室的电极反应式为:_________,图示中氢氧化钠溶液质量分数a%与b%的关系是____________(填字母)。 A. a%=b% B. a%﹥b% C. a%﹤b% ③甲中的离子交换膜为____(填“阳离子交换膜”或“阴离子交换膜”)。 (3)氯碱工业的产物NaOH与不同物质反应可以生成不同的盐。已知常温下,浓度均为0.1 mol/L的4种钠盐溶液pH如下表:
下列说法中,不正确的是____(填字母) a.向氯水中加入NaHCO3,可以增大氯水中次氯酸的浓度 b.四种溶液中,水的电离程度最大的是NaClO c.常温下,相同物质的量浓度的H2SO3、H2CO3、HClO,pH最大的是H2SO3 d.NaHSO3溶液中离子浓度大小顺序为c(Na+)> c(H+)>c(HSO3-) >c(SO32-)>c(OH-) |
第8题
| A~H是初中化学常见的8种物质,它们在一定条件下转化关系如下: ①A+B→C ②C+D→B+E ③F (1)上述③中将黑色固体G加入到F的溶液中,观察到有气体生成.该气体的化学式为______;该反应的化学方程式为______. (2)③反应的基本类型分别为______. (3)写出①、②反应的化学方程式______、______. (4)上述物质中属于氧化物的是______(填字母代号). |
第9题
| A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件及部分产物均未列出)。
(1)若A、D、E是短周期的非金属单质,且 A、D所含元素同主族,A、E含元素同周期,已知D单质在电子工业中有重要作用,则D的原子结构示意图为________;F的分子构型为________;反应①的化学方程式为__________________。 (2)若A、D为常见金属单质,且加热时A、D才能溶解在E的浓溶液中,写出反应③的化学方程式_ _________________;足量的A与B溶液充分反应后,生成物C中金属阳离子的检验方法为__________________;若以惰性电极电解B的水溶液,当阴极增重9.6g时,阳极生成气体在标准状况下的体积为________,写出电解B的水溶液的离子方程式__________________。 |
第10题
| 在一定的浓度范围内,该植物根系对该物质的吸收速率随浓度增加而增加,当达到P点后吸收速率不再增加。有人认为这种现象可表明该植物根系对该物质的吸收方式为主动吸收,也有人认为是被动吸收,请设计一个实验加以确定。 |
|
| (1)设计实验步骤;____________。 (2)预测实验结果并分析;______________。 |
第11题
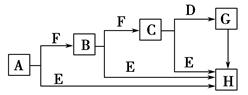 (1)下列对C的结构、性质推断中不正确的是 ()。(2)A的原子结构示意图为______________,H的电子式为______________,E的结构式为____________________。(3)C和E反应生成H的离子方程式为__________________,反应中氧化剂与还原剂的物质的量之比为______。
(1)下列对C的结构、性质推断中不正确的是 ()。(2)A的原子结构示意图为______________,H的电子式为______________,E的结构式为____________________。(3)C和E反应生成H的离子方程式为__________________,反应中氧化剂与还原剂的物质的量之比为______。A.久置于空气中会变成白色
B.具有强氧化性
C.晶体中存在离子键与非极性键
D.是一种碱性氧化物