 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
由下列反应计算Cl的电子亲和能: △rHmθ/(kJ.mol-1) (1)Rb(s)+1/2Cl2===RbCl
由下列反应计算Cl的电子亲和能: △rHmθ/(kJ.mol-1) (1)Rb(s)+1/2Cl2===RbCl -433 (2)Rb(s)===Rb(g) 86.0 (3)Rb(g)===Rb+(g)+e- 409 (4)Cl2(g===2C1(g) 242 (5)Cl-(g)+Rb+(g)===RbCl(s) 一686
 答案
答案






 (NaCl,s)。
(NaCl,s)。 O2(g)→O(g) △H3=249 kJ.mol-1 Mg2+(g)+O2-(g)→MgO(s) △H4=一3 916 kJ.mol-1 Mg(s)+
O2(g)→O(g) △H3=249 kJ.mol-1 Mg2+(g)+O2-(g)→MgO(s) △H4=一3 916 kJ.mol-1 Mg(s)+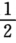 O2(g)→MgO(s) △H5=一602 kJ.mol-1
O2(g)→MgO(s) △H5=一602 kJ.mol-1



















