 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为: 2FeSO4 ="===" Fe2O3 +SO2↑+SO3↑为检验FeSO4高
| 工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为: 2FeSO4="===" Fe2O3+SO2↑+SO3↑ 为检验FeSO4高温分解的产物,进行如下实验: ①取少量FeSO4高温分解得到的固体,加一定量稀盐酸溶解,向该溶液中加入适量的KSCN溶液,观察溶液颜色的变化以检验Fe3+是否存在。 ②将FeSO4高温分解产生的气体通入右图所示的装置中,以检验产生的气体中是否含有SO2和SO3。请回答以下问题:
(1)写出用KSCN检验Fe3+的离子方程式____。 (2)装置I中试剂为氯化钡溶液,进行操作②时氯化钡溶液中有白色沉淀产生。甲同学说,这个白色沉淀可能是BaSO4和BaSO3的混合物;乙同学说,这个白色沉淀是BaSO4;丙同学说,这个白色沉淀是BaSO3。请你设计一个简单的实验帮他们加以鉴别。 ____ 你认为上述哪一位同学的观点正确?____ (3)装置II中试剂为品红溶液,其作用是____,品红溶液中可观察到现象是____。 (4)装置III中试剂为NaOH溶液,其目的是____。 |
 答案
答案







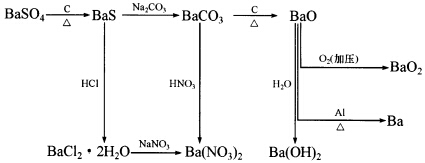 (1)现拟从重晶石制备BaCl2.2H2O。应该采用哪些步骤?写出其化学方程式,并说明完成反应的理由。 (2)为何不能用BaS与硝酸作用直接制备Ba(NO3)2? (3)为何工业上不采用BaCO3直接加热分解方法制备BaO?
(1)现拟从重晶石制备BaCl2.2H2O。应该采用哪些步骤?写出其化学方程式,并说明完成反应的理由。 (2)为何不能用BaS与硝酸作用直接制备Ba(NO3)2? (3)为何工业上不采用BaCO3直接加热分解方法制备BaO? 2NaOH+Cl2↑
2NaOH+Cl2↑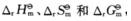 ,并说明通入O2的目的?
,并说明通入O2的目的?



















