 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试述Ga、In、Tl和Ge、Sn、Pb氧化态变化规律的相似性,并阐明原因。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“试述Ga、In、Tl和Ge、Sn、Pb氧化态变化规律的相似性,并阐明原因。”相关的问题
更多“试述Ga、In、Tl和Ge、Sn、Pb氧化态变化规律的相似性,并阐明原因。”相关的问题
第1题
不参考有关数据,请你预测下列各组元素的电负性并按递增的顺序排列。 (1)C,N,O; (2)S,Se,Cl; (3)Si,Ge,Sn; (4)Tl,S,Ge
第4题
请按照第一电离能递增的顺序排列下列几组原子。 (1)Be,Mg,Ca; (2)Te,I,Xe; (3)Ga,Ge,In
第5题
常用氢化物原子化法测定As、Sb、Bi、Ge、Sn、Te等元素,采用的还原剂是()。
A.Zn
B.NaBH4
C.Na2S2O3
D.H2
第7题
下列说法是否正确,并说明原因。
(1)S4O2-6中有两个S的化合价是0,另两个S的化合价则是+5,所以S4O2-6中S的氧化值也分别为0和+5。
(2)在电对Sn2+/Sn的溶液中,插入一根铜线,在电极和铜线间接上伏特计,指针发生偏转,测量值就是该电对的绝对电极电势。
(3)Nernst方程表明浓度对电极电势有着直接的影响,改变电对物质的浓度,电对电极电势或电池的电动势一定会发生相应的改变。
(4)电对
(5)某元素的中间氧化值M,且知该元素的电势
(6)因为
第8题
在298K时,将含有Sn(ClO4)2和Pb(ClO4)2的某溶液与过量的粉末状Sn-Pb合金一起振荡后,测得溶液中平衡浓度之比[Pb2+]/[Sn2+]为0.46。已知
 =-0.126V,计算
=-0.126V,计算
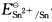 值。
值。
第9题
下列各对物质中哪一个酸性较强?说明理由。
(1) EFe(H2O)6]3+和[Fe(H2O)62+
(2) [A1(H2O)6]3+和Ga(H2O)63+
(3) Si(OH)4和Ge(OH)4
(4) HClO3和HClO4
(5) H2CrO4和HMnO4
(6) H3PO4和H2SO4