 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
取某地水样100.00ml,用氨性缓冲溶液调节至PH=10,以EBT为指示剂,用0.009434mol/L EDTA标准溶液滴定至终点,消耗9.70ML。计算水的总硬度(请分别用ppm和度为单位来表示计算结果)。另取同样水样100.00ml,用NaOH条件PH值至12.5,加入钙指示剂,用上述EDTA标准溶液滴至终点,消耗8.10ml,试分别求水样中钙离子和镁离子的含量。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“取某地水样100.00ml,用氨性缓冲溶液调节至PH=10,以EBT为指示剂,用0.009434mol/L EDTA标准溶液滴定至终点,消耗9.70ML。计算水的总硬度(请分别用ppm和度为单位来表示…”相关的问题
更多“取某地水样100.00ml,用氨性缓冲溶液调节至PH=10,以EBT为指示剂,用0.009434mol/L EDTA标准溶液滴定至终点,消耗9.70ML。计算水的总硬度(请分别用ppm和度为单位来表示…”相关的问题
第1题
用阳极溶出伏安法测定水样中的Pb2+、Cd2+、Cu2+含量。取水样4.00ml,加入到盛有46.0ml支持电解质溶液的电解池中,通2minN2,静置30s后将工作电极的电位向正方向扫描,测得Pb2+、Cd2+、Cu2+的溶出峰高分别为12mm、26mm、18mm。在上述溶液中加入0.10mlPh2+(10.00mg/L)、Cd2+(2.00mg/L)、Cu2+(5.00mg/L)的标准溶液,同样进行富集和溶出,测得溶出峰的峰高分别为20mm、45mm、32mm,试计算水样中Pb2+、Cd2+、Cu2+的含量。
第2题
某一有机酸(H2A)的 =4.19,
=4.19, =10.75,称取该酸纯固体样品2.9120g,配制100.00mL溶液。取此溶液25.00mL,用0.1012mol·L-1NaOH的滴定,消耗24.36mL,计算该有机酸的摩尔质量。本次滴定分析应当选用什么为指示剂?
=10.75,称取该酸纯固体样品2.9120g,配制100.00mL溶液。取此溶液25.00mL,用0.1012mol·L-1NaOH的滴定,消耗24.36mL,计算该有机酸的摩尔质量。本次滴定分析应当选用什么为指示剂?
第3题
测定某奎宁制剂中奎宁药物(C20H24O2N2,

第4题
称取0.1325g含ZrO2和HfO2并含其他杂质的混合物样品,用适当方法将ZrO2和HfO2同时与混合物中的其他杂质分离开后,再称重得ZrO2和HfO2共0.1194g。再将所得氧化物溶解,配制成100.00mL金属离子溶液。取25.00mL此溶液,用0.01000mol·L-1EDTA溶液滴定,用去21.67mL,求样品中ZrO2和HfO2的质量分数。已知ZrO2和HfO2的相对分子质量分别为123.2和210.5。
第5题
第6题
准确移取水样100mL.用0.01000mol/L硝酸银溶液滴定,消耗3.00mL.计算水中氯的含量。 [MCCl)=35.45g/mol]
第7题
取100.0mL水样,经过阳离子交换树脂后,Ca2+和Mg2+被交换至树脂上,流出液用0.1000mol·L-1的NaOH标准溶液滴定,用去10.00mL,试计算试样中水的硬度。
第8题
将0.167 5 g铁配制成100.00mL FeS04溶液,用0.100 0 mol. L -1 Ce(S04)2标准溶液滴定。铂电极作指示电极,SCE电极作参比电极,当加入20.00 mL Ce(SO4):标准溶液时,电池的电动势是多少?化学计量点的电动势是多少?
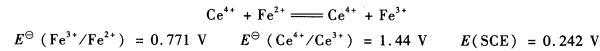
第9题
第10题
用碘量法测定水中硫化物时,取水样100ml,经预处理后分别测得吸收瓶1消耗Na2S2O3溶液5.35ml,吸收瓶2消耗Na2S2O3溶液8.69ml,空白消耗Na2S2O3溶液9.07ml,已知Na2S2O3标准溶液浓度为0.0098mol/L,硫离子的摩尔质量为16.03,试求水样中硫化物的浓度。
第11题
A.结果偏低
B.产生随机误差
C.产生系统误差
D.产生过失误差